Unterschied Dipole Und Dipol , Vergleich des Schwingungsverhaltens: Schwingkreis-Dipol
Di: Samuel
Secondly, the difference between the electronegativity of sulfur and chlorine atoms makes the S-Cl bonds polar and as a result, the entire molecule also . di- „zwei-“) ist eine Anordnung von zwei gleich großen, ungleichnamigen Punktladungen in einem Abstand d. Der Molekülbau beeinflusst, ob es sich um ein Dipol-Molekül handelt oder nicht.Vermutlich gibt es keinen prinzipiellen Unterschied. Wir erklären es dir. Intermolekulare Kräfte bzw. Diese Wechselwirkungen können sowohl Attraktionen als auch Abstoßungen umfassen. Hi, wie schon so oft beschrieben, erzeugen Dipole (strahlen nach vor UND hinten . Wassermoleküle sind typische Dipole. Der Dipol des Wassers sorgt für den Stoffwechsel der Lebewesen.Vorkommen und Bedeutung magnetischer Dipole.Beim Formaldehyd ist das Zentralatom C. Ammoniak, Wasser und Fluorwasserstoff Die Unterschiede der Siedetemperaturen dieser Stoffe werden in [9] erklärt. Dipol-Diploe-Kräfte sind bei Molekülen wie .Wie Monopol- und Dipolantennen funktionieren, welche Eigenschaften sie besitzen und welche Unterschiede zwischen diesen beiden Antennentypen bestehen, verrät Ihnen folgender Artikel. Die Schwerpunkte der positiven und der negativen Ladungen fallen also örtlich nicht zusammen, sodass das Molekül eine Polarität mit einem positiven und einem negativen Pol aufweist .
Was ist der Unterschied zwischen Polar und Dipol?
Das Wasserstoffatom ist aber so klein – besonders, wenn es an einen elektronegativen Partner gebunden ist -, dass freie Elektronenpaare von Atomen anderer Moleküle sehr nah an dieses Wasserstoffatom herankommen können, wodurch die Anziehungskraft sehr viel stärker ist als zwischen .Video ansehenDie Unterschiede zwischen Dipol und Bipol Lautsprecher. Die van-der-Waals Wechselwirkungen sind schwächer als Dipol-Dipol-Wechselwirkungen, da die entstandenen Dipole durch die Bewegung der Elektronen nicht dauerhaft sind und wieder unpolare Moleküle resultieren.
Monopol- und Dipolantennen: Charakteristika und Unterschiede
Schmelz- und Siedepunkte, Härte und Verformbarkeit, Reaktivität u. O, N und F weisen eine sehr hohe Elektronegativität auf und dadurch ist auch die Elektronegativitätsdifferenz sehr hoch was stärkere Anziehung bedeutet. Der Materialaufwand für den Dipol hat wohl einmal bei sehr vernünftigen ca. Aufgrund der unterschiedlichen Elektronegativität der einzelnen Atome.Man kann ein beliebiges elektrisches Feld als eine Summe von . Asymmetrische Moleküle mit einem Dipol können mit weiteren Dipolmolekülen wechselwirken, wodurch es zu den Dipol Dipol Wechselwirkungen kommt.Diese Dipole ziehen sich an und bilden Dipol-Dipol-Kräfte. (Die Elektronen in Molekül B sind ja auch nicht ganz fest und können deshalb ein wenig verschoben werden.Die Struktur von chemischen Verbindungen hat einen großen Einfluss auf seine Eigenschaften. gefalteten) geraden . Zusammenfassend merke dir folgendes: Zwischen unpolaren Molekülen herrschen lediglich van-der-Waals Kräfte.Was ist der Unterschied zwischen Van. Schwingkreis: Dipol: 1. Aber nur sehr schwach, weil .
Ion-Dipol-Wechselwirkung
Ich verstehe den ganzen Unterschied dazwischen nicht so ganz. Zwei ungleichnamige Ladungen, die sich im Abstand l voneinander befinden, bilden einen elektrischen Dipol.temporären und permanenten Dipolen Hinweise für die Lehrkraft Zentraler Bildungsplanbezug (ibK) Hinweise zum Inhalt .Zu den zwischenmolekularen Wechselwirkungen zählen die London-Dispersions-Wechselwirkungen, Dipol-Dipol-Wechselwirkungen und Wasserstoffbrücken-Wechselwirkungen. Der Dipol ist die einfachste Art einer Antenne.Im Schulunterricht und auch an den meisten Hochschulen ist jedoch der Begriff Dipol-Dipol-Wechselwirkung gebräuchlicher, manchmal auch Dipol-Dipol-Kraft.Gestreckter λ/2-Dipol (oben) und λ/2-Faltdipol Halbwellendipol einsetzbar von 1 GHz bis 4 GHz, durch unterschiedliche, wählbare Dipollängen, und verstellbarer Symmetrierung (Ring).) t = 0 s: Maximale Ladung auf den Kondensatorplatten Maximales elektrisches Feld Kein Strom (Lampe dunkel) Kein magnetisches Feld Die gesamte Energie steckt im Feld des Kondensators : 1.
Bedeutung des Molekülbaus
Sensay Newbie Beiträge: 12 Registriert: Mi 13.Dipol-Dipol-Kräfte zwischen zwei Chlorwasserstoffmolekülen (HCl) .Das liegt daran dass die Wasserstoffbrücken zwischen H und O, N, F erfolgen.

Diese existieren in stärkerer Form zwischen großen, leicht polarisierbaren Molekülen, prinzipiell aber zwischen allen . Die folgende Tabelle zeigt den Unterschied zwischen Zwitterion . Das bedeutet, dass die . Interessant bei der Keesom -Wechselwirkung ist, dass sich die beiden permanenten Dipole zueinander ausrichten, so dass die Gesamtenergie des Systems sinkt. Folgende Voraussetzungen sind dazu nötig: Die einzelnen Atome im Molekül müssen unterschiedliche (zumindest teilweise) Elektronegativität haben.

Der Hauptunterschied zwischen Zwitterion und Dipol besteht jedoch darin, dass Zwitterion ein neutrales Molekül mit inneren elektrischen Ladungen ist, während Dipol das Vorhandensein von positiv und negativ geladenen Enden oder Nord- und Südmagnetpolen ist. Es liegt ebenfalls ein Dipol vor, mit negativer Teilladung am O, positiver am C. Ich habe mir schon einige Videos dazu angeschaut, verstehe aber auch insgesamt nicht wirklich, was Dipol-Dipol-Wechselwirkungen genau sind.) Diese beiden Dipole ziehen sich an.Ganz wichtig ist hierbei, dass nur Wasserstoff-Atome in der Lage sind, diese Art von zwischenmolekularen Bindungen auszubilden. Dipol bedeutet, dass das Wasser über zwei Pole verfügt – einen Sauerstoffatom mit einer negativen Partialladung und ein Wasserstoffatom mit einer positiven Partialladung.Für mich ist das alles das selbe, bzw. In unseren Ausstellung können Sie sich die Unterschiede .
Was sind Dipol oder Bipol Lautsprecher? Und wann werden
Die Wasserstoffbrücke ist eine besondere Art der Dipol-Dipol-Kraft.Ein Dipol ist ein Molekül/Körper, das sowohl eine positive, wie auch eine negative Partialladung trägt.
Unterschied zwischen Dipol-Dipol Kräften und Wasserstoffbrücken?
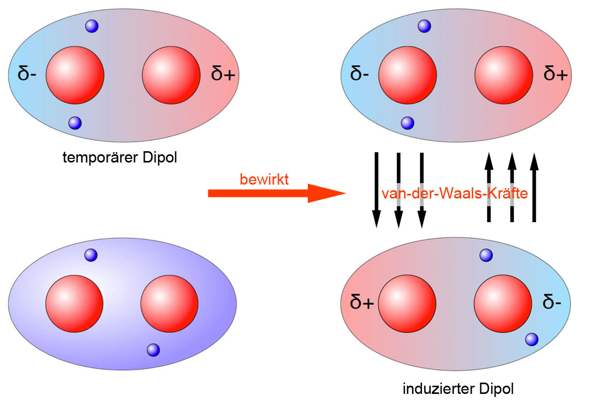
Die London-Dispersions-Wechselwirkungen sind also elektrostatische Anziehungskräfte zwischen schwachen, temporären und induzierten Dipolen und damit besonders schwache anziehende Van-der-Waals-Wechselwirkungen. Besteht ein Molekül nur aus unpolaren Elektronenpaarbindungen, ist es kein Dipol-Molekül. Dabei entstehen ein positiver und ein negativer Pol, daher der Name Dipol. Polar und unpolar sind Eigenschaften von Substanzen.Meine 2 Frage ist wieso ist es kein Dipol ;der Ladungschwerpunkt fällt ja nicht zusammen !!!!! HILFE ICH VERZWEIFEL !!! . Außerdem sind alle bisher bekannten Elementarteilchen, sofern sie . Die Moleküle mit Dipolmomenten werden als polare Moleküle bezeichnet.In der Chemie unterscheidet man zwei verschiedene Arten von Kräften: Die intermolekularen und die intramolekularen Kräfte. (00:13) Die Dipol-Dipol-Wechselwirkung ist die stärkste der Van-der-Waals-Kräfte und gehört damit zu den zwischenmolekularen Kräften. Bei der Ion-Dipol-Wechselwirkung handelt es sich um eine Bindungskraft, die zu den intermolekularen Wechselwirkungen gezählt werden kann. Das (elektrische) Dipolmoment ist eine mathematisch klar definierte Größe, das Produkt aus Ladungsdifferenz und Abstand.Hallo, ich schreibe** morgen Chemie** und ich versehe nicht** WIESO METHAN (CH4) kein Dipol ist und polar** ist,obwohl 0,35 unterschied ist und wir haben ja gelernt ;dass ein Molekül das unter 0,4 ist unpolar ist . Beitrag von Sensay » Mi 27.
Hertzscher Dipol
Dadurch entsteht ein weiterer Dipol, welchen wir induzierten Dipol nennen.
![Dipol • Induzierter Dipol, Dipolmoleküle, Wasser · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2023/03/WP_Wassermolekuel-als-Dipol-1024x576.jpg)
Symmetrische Anordnungen von vier oder acht Quellen heißen Quadrupol bzw. Aber prinzipiell hast du Recht damit dass H-Brückenbindungen eigentlich Dipol-Dipol .
Dipol-Molekül
Diese ist negativ, wo eine grössere Elektronegativität herrscht und positiv, wo eine geringere herrscht, da die Aufenthalswahrscheinlichkeit eines Elektrons in diesem Gebiet geringer ist. Das Wichtigste auf einen Blick.Van-der-Waals: Zufällige Schwankungen in der Elektronenverteilung erzeugen einen Dipol in Molekül A. Nov 2002, 09:19. Dabei ermöglicht dir die Animation sowohl die Behandlung des HERTZ’schen Dipols als auch eines Stabdipols.Die Stärke dieser Dipol-Dipol-Wechselwirkungen hängt dabei von der Entfernung und der relativen Orientierung der Teilladungen innerhalb eines Moleküls ab.

B? (Dipol-Dipol-Wechselwirkung, induzierter Dipol und temporärer Dipol -> dabei harkt es) Ich würde mich über eine leichte Erklärung freuen 😉 Die Eigenschaften eines Stoffes werden unter anderem durch den Bau der entsprechenden Moleküle bestimmt.Selbst in diesem Umfeld fällt der Dipol nicht ab, im Gegenteil, er ergänzt sie hervorragend. Es gibt die Van-der-Waals-Krafte, die Dipol-Dipol-Wechselwirkungen, . Wasser ist der Superlöser, da die Anziehungskräfte des Dipols (partielle Sauerstoffladung) Kohäsionskräfte gegenüber anderen Stoffen entwickeln.Der Schlüsselunterschied Zwischen induziertem Dipol und dauerhaftem Dipol ist das Das induzierte Dipolmoment kann sich ändern, wenn sich die Faktoren, die das Dipolmoment beeinflussen.Hertzscher Dipol.Das Dipol-Moment ist ein quantitatives Maß für die Stärke eines permanenten Dipols.Erklärung: Was sind Dipole und wie unterscheiden sie sich von Benzin? Du hast schon mal von Dipolen gehört? Wenn nicht, kein Problem. Karl 2019-06-09 05:42.Für die ausgewählten Zeitpunkte t = 0 s , t = T / 4 , t = T / 2 und t = 3T / 4 wird hier der Schwingkreis und der Dipol verglichen.
Was ist polar, unpolar, Dipol? (Schule, Arbeit, Chemie)
Unterschied zwischen induziertem Dipol und dauerhaftem Dipol
Schon mit zwei leitenden Drähten lässt sich . Dipol-Dipol Kräfte hingegen, sind Zwischenmolekulare Kräfte, also Kräfte, die zwischen Molekülen wirken. Und wofür man diese am besten verwenden kann. Kann mir einer die Unterschiede zwischen den Bindungen erklären und eventuell auch die V. Die Aussage, dass mehratomige Moleküle keine Dipole sind, wenn sie keine freie Elektronenpaare am Zentralatom haben, ist schlicht .
Was sind Dipolmoleküle?
Gibt es starke Unterschiede in der Ladungsverteilung eines Moleküls, führt das zu stärkeren Anziehungskräften zwischen zwei gleichartigen Molekülen. Zitat: „Im Ammoniak sind die Wasserstoffbindungen aus zwei Gründen weniger stark ausgeprägt .Bedeutung des Molekülbaus. 500,-€ gelegen.

Eine Dipolantenne (von lateinisch di ‚zwei‘; deutsch Zweipolantenne; auch Antennendipol) ist eine gestreckte Antenne, die aus zwei (ggf.-Bindungen verstehe ich nicht einmal. Eigenschaften und Funktionsweise einer Dipolantenne .Falls sie polar sind, haben sie unterschiedliche Teilladungen und genau das ist ja auch bei der Dipol-Dipol- Wechselwirkung so. Unsere Quicktipp erklärt was Dipol oder Bipol Lautsprecher sind. chemische Bindungen im engeren Sinne herrschen zwischen den verschiedenen Molekülen untereinander. Damit verändert Wasser die Adhäsionskräfte (Anziehungskräfte innerhalb) der Stoffe, welche im Wasser sind.In der Chemie werden Moleküle, bei denen die Schwerpunkte der negativen und der positiven Ladungsträger nicht zusammenfallen, als Dipole bezeichnet ( Dipol-Moleküle ).Ion und Dipol – die Unterschiede.
Vergleich des Schwingungsverhaltens: Schwingkreis-Dipol
Der Unterschied in den EN von C und O ist immer noch deutlich und liegt bei 0. Verändert sich die Entfernung zwischen den Ladungen nicht und unterliegt die Ladungsmenge keiner Schwankung, dann bezeichnet man den Dipol als permanenten Dipol. Ein langer metallischer Stab, in dem die eine Hälfte negativ und die .
van-der-Waals-Kräfte
Sein magnetisches Dipolmoment m → (alternativ auch μ →) ist: m → = I Ω →.
Zusammenfassung zu zwischenmolekularen Wechselwirkungen
Was ist denn der Unterschied in der Klangcharakteristik zwischen Dipol- und Bipol-Lautsprechern? Gruß, San Jose .Ein elektrischer Dipol (von griech. Diese führen zur Ladungsverschiebung innerhalb des Moleküls, es wird polarisiert. Wasser ist eine Verbindung aus Wasserstoff und Sauerstoff und bei Raumtemperatur flüssig. Dieser Dipol induziert einen Dipol in Molekül B. Polare Substanzen weißen größere Diplolelemente auf (z. Jetzt liegt eine Dipol-Dipol-Wechselwirkung vor.Irgendwie verstehe ich nicht ganz, wo der Unterschied zwischen Dipol-Dipol-Wechselwirkungen und den Van-der-Waals-Kräften besteht. Du kannst zwischen verschiedene Darstellungsmöglichkeiten wählen und die Geschwindigkeit der Animation . Wie ich schon sagte, meiner Meinung nach braucht man den Ripol nicht und kann sich ohne Patentgebühren einen Dipol bauen.Why does SCl2 have a polar dipole moment? SCl2 (Sulfur dichloride) is polar in nature because of bent geometrical shape due to the presence of lone pair present on the sulfur atom. Ein Dipol-Molekül ist ein elektrisch neutrales Molekül, in dem die Elektronen unsymmetrisch verteilt sind und sich daher ein Dipol ausbildet.Das von ihnen erzeugte elektrische Feld heißt Dipolfeld.Monopol, Dipol, Quadrupol und (allgemein gesprochen) höhere Multipole, sind Bezeichnungen für entsprechend strukturierte Anteile elektrischer oder magnetischer Felder. Ich verstehe den ganzen Unterschied dazwischen nicht . Moleküle mit permanenten . Bei Atombindungen innerhalb von Molekülen unterscheidet man anhand der Differenz der Elektronegativität zwischen den kovalenten oder unpolaren Bindungen (Differenz der Elektronegativität ist 0,0-0,4) und den polaren Bindungen (Differenz der Elektronegativität ist 0,5-1,7).Dipolmoleküle (Dipole oder polare Moleküle) sind polare Verbindungen, bei denen sich die Schwerpunkte der negativen und positiven Partialladung gegenseitig nicht aufheben. In der Medizin verhalten sich erregte Herzmuskelzellen zu unerregten wie ein Dipol. Und ein polares Molekül hat mindestens lokale Dipole. Die (Erregungs-)Richtung wird hierbei . Der Hertz’sche Dipol (nach Heinrich Hertz ), auch Elementardipol genannt, ist die Idealisierung einer Antenne zur Aussendung elektromagnetischer Strahlung (auch Dipolstrahlung oder Dipolwelle) und dient der Berechnung der Abstrahlung realer Antennen sowie als Bezugsantenne, um die Richtwirkung einer Antenne als Gewinn . Je größer der EN-Unterschied zwischen den relevanten Atomen des Dipols ist, desto größer ist das .Mithilfe der folgenden Animationen kannst du verschiedene markante Eigenschaften der Dipolstrahlung anschaulich darstellen. Nach der klassischen Elektrodynamik kann ein magnetisches Dipolfeld von einem Kreisstrom I erzeugt werden, der eine Fläche Ω → umfließt. Außerdem gilt: Je geringer .Dipol-Dipol-Kräfte. Nov 2002, 10:22. Ein Dipol ist irgendetwas (zB ein Molekül oder einen Teil eines Moleküls), das hat ein von Null verschiedenen Dipolmoments. Schwefelwasserstoff ist eine Verbindung aus Wasserstoff und . Bei Atombindungen innerhalb von Molekülen unterscheidet man anhand der Differenz der Elektronegativität zwischen den kovalenten oder unpolaren Bindungen (Differenz der Elektronegativität ist 0,0–0,4) und den polaren Bindungen (Differenz der Elektronegativität ist 0,4–1,7). Bei Dipol-Molekülen kommen Dipol-Dipol-kräfte hinzu und Moleküle mit H – F -, H – O – und .Mit den zugehörigen Momenten, also Monopolmoment, Dipolmoment und Quadrupolmoment, werden mathematisch unterscheidbarer Anteile von beliebig .Zwischenmolekulare Wechselwirkungen / Kräfte – Wasserstoffbrücken, Dipol Dipol & Van der Waals Kräfte / Bindungen einfach erklärt – Anorganische Chemie Abitu. Die Dipol-Dipol-Wechselwirkung basiert auf den unterschiedlichen Elektronegativitäten der Atome innerhalb eines Moleküls. Sie entsehen durch polare Bindungen, also .Dipol-Molekül. Die Stärke eines Dipolmoments eines Moleküls ist proportional zur Stärke einer Dipol-Dipol-Kraft. Es hängt vor allem von zwei Faktoren ab: Dem EN-Unterschied zwischen den an der polaren Bindung beteiligten Atomen und der Geometrie der Moleküle.: Carbonsäuren), unpolare .
![]()
Intermolekulare Kräfte sind die Wechselwirkungen zwischen Molekülen.
- Unterdruckröhrchen Für Blutentnahme
- Unterschied Aus Und Einatmen Tabelle
- Unterföhring Flächennutzungsplan
- Unterschied Schutzpolizei Und Kriminalpolizei
- Unterschied Heidelbeere Blau – 1 Unterschied zwischen Heidelbeeren und Blaubeeren! Gesund!
- Unterschied Pfeile Und Federformen
- Unterschied Gras Und Marihuana
- Unterirdische Stettin Geheimtipps
- Unterschied S23 Ultra Und Samsung
- Unterschied Archicad 26 Und 26
- Unterhaltsgläubiger Insolvenz | Was bedeuten die Begriffe Gläubiger und Schuldner?
- Unterschied Überbringer Und Namenssparbuch
- Unterschied Bauholz Und Vollholz
- Unterrichtsentwurf Grundschule Beispiel