Tofersen Als Medikament : SOD1-ALS: Tofersen verbessert molekulare Anzeichen der Krankheit
Di: Samuel
Elmas stellte eine Auswertung von Anwendungsdaten bei 24 ALS-Kranken vor, die an diesem Programm teilnahmen. Die ALS-App wird für das Monitoring der Tofersen-Behandlung zuerst an .Amyotrophe Lateralsklerose: EMA empfiehlt Tofersen bei Patienten mit SOD1-Mutationen. Der primäre Endpunkt (Änderung des ALSFRS-R-Fragebogen-Scores) wurde . The committee will meet virtually on March 22 to review data associated with Biogen’s new drug application. Der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittelagentur (EMA) hat auf seiner Sitzung im Februar 2024 insgesamt 10 Arzneimittel bzw. We conducted a phase 1–2 ascending-dose trial evaluating tofersen in adults with ALS due to SOD1 mutations.
ALS Association Submits Public Comments in FDA Review of Tofersen
Es ist eine neue Therapie für Menschen mit amyotropher Lateralsklerose und Mutationen im Superoxid-Dismutase-1-Gen (SOD1-ALS).Tofersen (Qalsody™) is an antisense oligonucleotide being developed by Biogen for the treatment of amyotrophic lateral sclerosis (ALS). Die Behandlung in der placebokontrollierten Studie erfolgt über sechs Monate. Dazu setzt die Universitätsmedizin Mannheim (UMM) das neuartige Gen . Veröffentlicht am: 23. Food and Drug Administration granted accelerated approval for QALSODY to treat amyotrophic lateral sclerosis (ALS) in adults who have a mutation in the superoxide . Dazu setzt die Universitätsmedizin Mannheim (UMM) das neuartige Gen-Medikament Tofersen bei ALS-Patienten mit einer Mutation der . Unsere Ambulanz ist Anlaufstelle für Patient*innen mit amyotropher Lateralsklerose (ALS), Spinale Muskelatrophie (SMA), Kennedy Erkrankung (SBMA) und anderen Motoneuronerkrankungen am Uniklinikum Bonn.Seit März 2022 werden in der ALS-Ambulanz der Berliner Charité zwei Patientinnen und ein Patienten mit dem Medikament Tofersen behandelt. Trotz der zahlreichen (medizinischen und bürokratischen) Hürden und Rückschläge, die auf dem Weg zur . Das Antioxidans Edaravone hatte in einer . Nach sechs Monaten Therapie habe sich eine . The Food and Drug Administration has conditionally approved a new ALS medicine in a decision likely to influence how other experimental treatments for the nerve-destroying disease are tested and reviewed.
ALS verlangsamen: UMM setzt neues Gen-Medikament ein
Background: The intrathecally administered antisense oligonucleotide tofersen reduces synthesis of the superoxide dismutase 1 (SOD1) protein and is being studied in patients with amyotrophic lateral sclerosis (ALS) associated with mutations in SOD1 (SOD1 ALS).Sobald Tofersen die EMA-Zulassung erhalten hat, kann jeder Mitgliedstaat sein eigenes Verfahren für die Bereitstellung des Medikaments auf dem lokalen Markt einleiten.
FDA Approves First ALS Treatment Via Accelerated Approval
Das Medikament namens Tofersen wurde für ALS-Patienten entwickelt, die Mutationen im SOD1-Gen aufweisen und an einer erblichen Form der ALS (familiäre ALS, FALS) erkrankt sind.The ALS Association submitted comments today to the FDA’s Central and Peripheral Nervous System Advisory Committee, urging it to recommend approval of tofersen for people with ALS linked to a SOD1 gene mutation.genetische Therapie bei der ALS. (Hinweis: Die Voraussetzungen gemäß § 2 Abs.In this cohort study, we investigated and reported the effect of tofersen on clinical outcome parameters (ALSFRS-R, progression rate, quality of life, adverse events), laboratory findings in CSF, and biomarkers (NfL in serum, pNfH in CSF) in a multicenter cohort of ALS patients (n = 24) in a “real-world” setting. Es hemmt das Gen der Superoxid-Dismutase 1 (SOD1), der zweithäufigsten genetischen Form der ALS.We confirmed a decrease of NfL .EMA: Empfehlung für 10 neue Medikamente, u. Die Dokumentation und Überwachung des Behandlungsverlaufs werden mit der ALS-App unterstützt. Es werden mehrere Verlaufsformen unterschieden. Accelerated approval is different than full approval in that treatments approved . Das Medikament Tofersen (Qalsody®, Biogen) hat eine Zulassungsempfehlung in der EU erhalten.Die EMA empfiehlt die Zulassung von Tofersen, Handelsname Qalsody, zur ALS-Therapie.In dem Interview berichtet Sonja Kämpfer von der Erkrankung ihrer Tochter Anna an FUS-ALS und vom komplizierten und steinigen Weg zur Diagnose und schließlich zur Therapie mit dem genetischen Medikament „Jacifusen“. Die Substanz Tofersen ist aktuell in einem speziellen Programm von Biogen für ausgewählte Patientinnen und Patienten mit amyotropher Lateralsklerose verfügbar, welche eine nachgewiesene Mutation im SOD1 . The medicine, known until now as tofersen, is only for ALS patients who have a specific .Tofersen ist das erste ASO-Medikament, das für die Therapie der ALS entwickelt wurde und hoffen lässt, dass es bei einigen Menschen mit ALS den Krankheitsverlauf eindämmen oder zumindest stark verlangsamen kann.ALS Association Funded Antisense Technology Behind Tofersen . Liebe Leserin, lieber Leser,2022 Ein Studienmedikament, das zur Behandlung einer seltenen, vererbten Form der amyotrophen Lateralsklerose (ALS) entwickelt wurde, verringerte die molekularen Anzeichen der tödlichen, lähmenden Krankheit und bremste die Neurodegeneration – .2024 : Herz-Kreislauf-Erkrankungen .
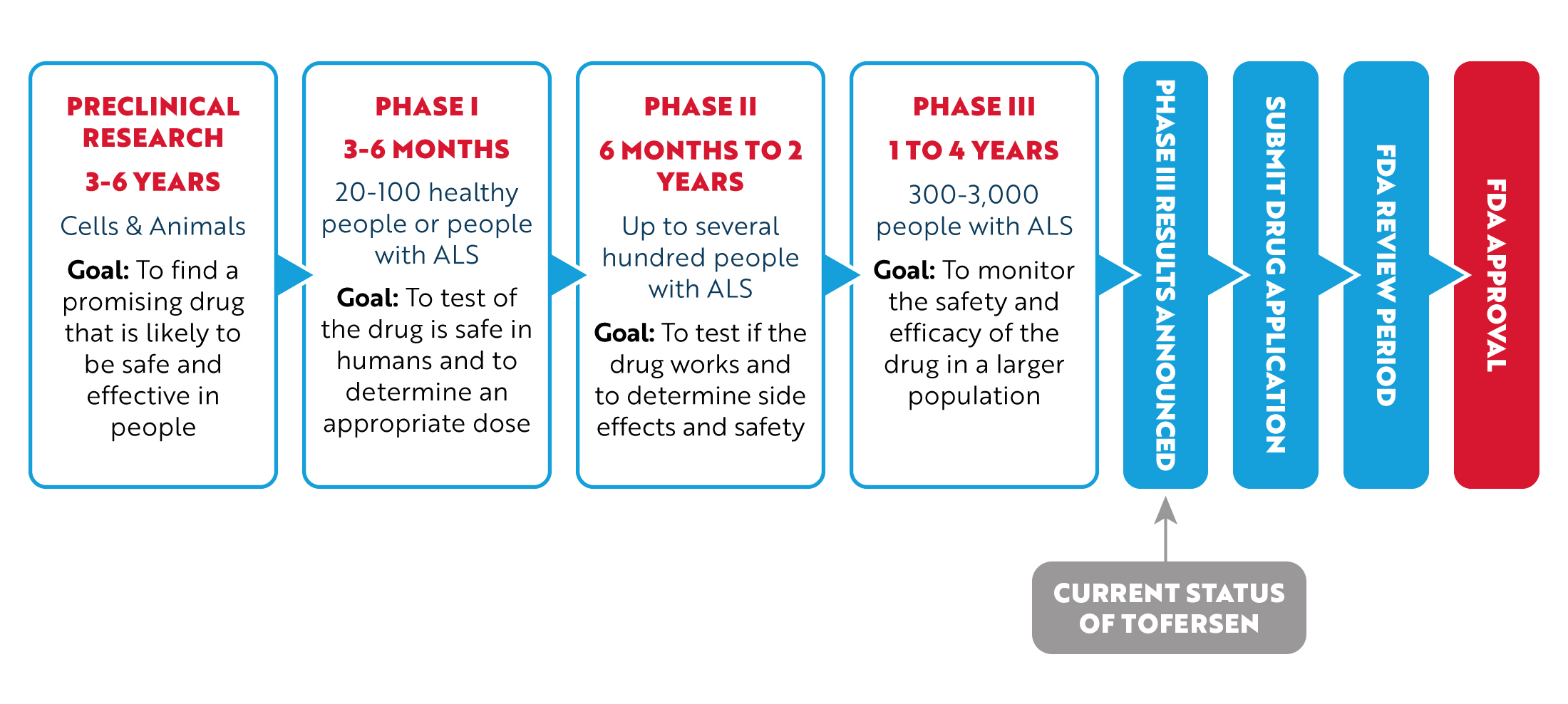
ALS-Medikament: Weg frei für Phase 3
Silver Spring – Die US-Arzneimittelbehörde FDA hat einen neuen Wirkstoff zur Behandlung der amyotrophen Lateralsklerose (ALS) zugelassen.23 February 2024.Digitale Medizin; Spezialisierte Behandlung; Cannabis-Medikamente; Publikationen; Über uns; Zur Stiftung; Über ALS; Kontakt; Tofersen reduziert Neurofilament – Erste Ergebnisse aus dem Härtefallprogramm publiziert.Die Amyotrophe Lateralsklerose (ALS) ist bisher nicht heilbar: Erkrankte leiden unter zunehmender Muskellähmung, die letztlich zum Tod führt. Die Therapie bestand in einer Injektion von Tofersen, einem Medikament des Biotech-Unter . Impfstoffe zur Zulassung . Influenza-Impfstoffe für Pandemien und eine ALS-Therapie. Erste Ergebnisse der zulassungsrelevanten Phase-IIIStudie VALOR zeigen dass der primäre Endpunkt – eine .

About QALSODY ® (tofersen) QALSODY ® (tofersen) is an antisense oligonucleotide (ASO) designed to bind to SOD1 mRNA to reduce SOD1 protein production.Das Medikament wird intravenös durch eine Infusion in der Studienambulanz verabreicht.

_0.jpg?h=2f03dbdf&itok=pmTN6jyg)
Tofersen3 Tofersen ist ein Medikament, das intrathekal (durch eine Injektion in den Rückenmarkskanal) verabreicht wird.
EMA empfiehlt Tofersen zur Therapie von ALS
Bei bestimmten Formen der ALS kann nun allerdings das Fortschreiten der Erkrankung verlangsamt werden.
ALS-Medikament .Tofersen ist ein innovatives Medikament, das darauf abzielt, genetische Informationen im Körper von ALS-Betroffenen zu beeinflussen. Die Amyotrophe Lateralsklerose (ALS) ist bisher nicht heilbar. Bei Arzneimitteln für seltene Leiden wie Qalsody kann dies im Durchschnitt zwischen 102 Tagen (Deutschland) und 1. Tofersen ist ein Antisense-Oligonukleotid, das in die SOD1-Proteinsynthese eingreift und so den Spiegel des mutierten Proteins reduziert. Thomas Meyer, Leiter der ALS-Ambulanz der Charité.Permission granted by Biogen. 1 AMHV müssen erfüllt sein) Datum des Zugangs der bestätigten. Qalsody (tofersen) is indicated for the treatment of adults with .

The most common .FDA Grants Accelerated Approval for QALSODY™ (tofersen) for SOD1-ALS, a Major Scientific Advancement as the First Treatment to Target a Genetic Cause of ALS .USA/Kanada: Hersteller nimmt ALS-Medikament Relyvrio vom Markt Amyotrophe Lateralsklerose: Relyvrio enttäuscht in Phase-3-Studie Amyotrophe Lateralsklerose: EMA empfiehlt Tofersen bei Patienten .
Neue ALS-Behandlungen 2022
Recently, the antisense oligonucleotide tofersen became the first gene-based therapy for ALS to receive accelerated approval in the USA for the treatment of SOD1-associated ALS based on the results of the VALOR trial and its open label extension published in 2022 []. In each dose cohort (20, 40, 60, or 100 mg), participants were randomly .
Tofersen
Das Interview wird geführt von Susanne Spittel, . Verband Forschender Arzneimittelhersteller vfa. April 25, 2023 • News Release. On 25 April 2023, tofersen was approved in the USA for the treatment of ALS in adults who have a mutation in the superoxide dismutase 1 (SOD1) gene.Team Motoneuronambulanz. Amsterdam – Die Europäische Arzneimittelagentur (EMA) hat die Zulassung des . In the 28-week randomized VALOR component of the trial, tofersen was associated with reduc-tions in the total concentration of SOD1 protein in CSF, an indirect marker of target . EMA has recommended granting a marketing authorisation in the European Union for a new therapy for the treatment of adult patients with amyotrophic lateral sclerosis (ALS), a rare and often fatal disease that causes muscles to become weak and leads to paralysis. Der amerikanische Arzneimittelhersteller Biogen hat das genetische Medikament Tofersen entwickelt, das gegen die Mutation SOD-1-Gen gerichtet ist und vor allem bei ALS-Patienten, die Mutationen in diesem Gen aufweisen und an einer erblichen Form der ALS (familiäre ALS) leiden eingesetzt werden kann.Amyotrophe Lateralsklerose (ALS): Vielversprechende Studienergebnisse.Tofersen (BIIB067) ist ein Antisense- Wirkstoff von Biogen, der sich in der klinischen Prüfung zur Behandlung von Menschen mit Mutation der Superoxid- Dismutase 1 bei amyotropher Lateralsklerose (SOD1-ALS) befindet.Erste Ergebnisse der zulassungsrelevanten Phase-III-Studie VALOR zu Tofersen, einem Prüfpräparat zu einem Antisense-Wirkstoff zur Behandlung von Patienten mit Mutation der Superoxid-Dismutase 1 bei amyotropher Lateralsklerose (SOD1-ALS), liegen vor. (Wirkstoff) Medizinische Indikation / Patientengruppe.This marks the first time the FDA . 2023) – The ALS Association commends the FDA for approving tofersen under the agency’s accelerated approval pathway for the treatment of people living with ALS connected to mutations in the SOD1 gene.Erprobung des Antisense-Oligonukleotids Tofersen bei SOD1-ALS. Das Medikament von Biogen ist für ALS-Patienten mit Mutationen im SOD1-Gen geeignet und verlangsamt hier die Progression dieser tödlichen neurodegenerativen Erkrankung.

für Patient:innen mit Alzheimer-Demenz, Krebs- und Autoimmunerkrankungen möglich. Zulassung von Tofersen empfohlen.2019 Eine Frühphasenstudie zur Behandlung von amyotropher Lateralsklerose (ALS) legt nahe, dass das experimentelle Medikament Tofersen (Qalsody) verträglich sein könnte, und in explorativen Ergebnissen wurde das Medikament mit einer möglichen . Diagnostik, Behandlung und Erforschung dieser Erkrankungen sind im Mittelpunkt . Tofersen is an antisense oligonucleotide that targets the production of superoxide dismutase 1, an enzyme whose mutant form is commonly associated with ALS. Gesprächspartner ist Prof. Die Behandlung erfolgte bei einer Patientin, die eine Mutation im Gen der Superoxiddismutase 1 (SOD1) aufweist. Methods: In this phase 3 trial, we randomly assigned adults with . Welche Medikamente auch in Deutschland auf den .Tofersen, sold under the brand name Qalsody, is a medication used for the treatment of amyotrophic lateral sclerosis (ALS). Laufzeit des Härtefall-. > Terminvereinbarung. Die amyotrophe Lateralsklerose, kurz ALS, ist eine chronisch – degenerative Erkrankung des zentralen Nervensystems ( ZNS ), die mit einer Atrophie der Skelettmuskulatur und Pyramidenbahnzeichen einhergeht. Tofersen ist ein Antisense-Oligonukleotid (ASO), das die Produktion des SOD1-Proteins reduzieren soll.Die Bedeutung des genetischen Screenings, die Implikationen für Angehörige, aber auch die Bewertung des Medikaments Tofersen stehen im Mittelpunkt dieser Folge des ALS-Podcasts.Liste der bestätigten Arzneimittel-Härtefallprogramme. Fortschritte u. März 2022 wurde in der ALS-Ambulanz der Charité erstmalig eine genetische Therapie bei einer ALS-Patientin durchgeführt.
Tofersen (Qalsody)
5% aller ALS-Patienten mit Mutationen im SOD1-genInsgesamt ist die Zulassung von Tofersen (Handelsname Qualsody) das erste Medikament gegen eine genetische Form der ALS (SOD1-ALS) und damit als medizinisch-wissenschaftlicher Durchbruch zu betrachten. Für mehr als 40 neue Medikamente dürfte 2024 eine Markteinführung in EU-Ländern in Betracht kommen.
SOD1-ALS: Tofersen verbessert molekulare Anzeichen der Krankheit
In einer Phase-1/2-Studie .In Deutschland haben ALS-Erkrankte mit SOD-1-Mutation seit März 2022 die Möglichkeit, sich im Rahmen des Early Access Programms mit Tofersen behandeln zu lassen. Ab 2020 sind Behandlung mit dem genetischen Medikament Tofersen sowie eine Studie zur Wirksamkeit des Medikamentes geplant. Anschließend wird eine offene Fortsetzungsstudie durchgeführt.Das Schweizer Unternehmen Neurimmune hat ein Medikament mit dem Namen „AP101“ entwickelt, um die schädlichen Ablagerungen von SOD1-Proteinen zu reduzieren.Tofersen (Qalsody ™ ) is an antisense oligonucleotide being developed by Biogen for the treatment of amyotrophic lateral sclerosis (ALS).
Thema Amyotrophe Lateralsklerose
Dabei handelt es sich um einen Antikörper, der fehlgefaltete SOD1-Proteine erkennt und somit die Bildung von SOD1-Aggregaten (Zusammenballungen von .März 2023, fand eine mehrstündige Beratung bei der US-amerikanischen Gesundheits- und Zulassungsbehörde „Food and Drug Administration“ (FDA) für eine zukünftige Zulassung des Medikaments . Bei Menschen mit ALS und Mutationen im SOD1-Gen (SOD1-ALS) steht seit Februar 2022 das Medikament Tofersen im Rahmen eines .
Tofersen bei SOD1-ALS: Ergebnisse der Phase-III-Studie
Here’s why: This would be the first use of accelerated approval in ALS.Tofersen is currently available in many other countries as part of an .081 Tagen (Estland) dauern 7 .Insgesamt ist die Zulassung von Tofersen (Handelsname Qualsody) das erste Medikament gegen eine genetische Form der ALS (SOD1-ALS) und damit als medizinisch-wissenschaftlicher Durchbruch zu .The advisory committee’s decision on tofersen represents a critical moment for everyone living with ALS and their loved ones – and for those who may be diagnosed in the future.It is administered as an intrathecal injection. In dieser Phase erhalten alle Patienten das Studienpräparat AP101 (open label extension, .Das Medikament kommt bei 2. FDA granted accelerated approval of QALSODY based on a reduction of neurofilament, a marker of neurodegeneration 1; Superoxide . This article summarizes the milestones in the .
- Tom Brady Girlfriend 2024 _ Who Is Veronika Rajek? Tom Brady Fans Aflutter as Model
- Tomates Französisch | die Tomate
- Tommy Shelby Wallpaper , Download Tommy Shelby Of Peaky Blinders Wallpaper
- Toilettenreinigung Mit Chlor , Ratgeber: So reinigen Sie ihren Abfluss richtig
- Tivoli Center Konstanz : Restaurant Tivoli-Center in Konstanz
- Tischaschenbecher Für Außenbereich
- Tischläufer 35 X 120 , Tischläufer günstig online kaufen
- Tödlicher Unfall Motorradfahrer
- Tontöpfe Kaufen In Der Nähe , Teramico
- Toolkit Windows 11 : ImDisk Toolkit
- Toilettenpapier Günstig : Toilettenpapier WC-Papier günstig bei Toilettenpapier 24