Thiosulfatlösung Stärke Nachweisen
Di: Samuel
Schritt: Das Thiosulfat (Oxidationszahl Schwefel: +II) zerfällt langsam in Verbindungen mit günstigerer . Blumes Bildungsserver für Chemie.Gegen Ende der Titration werden 2 ml Stärke-Lösung R zugesetzt und bis zur mindestens 2 min lang bestehenbleibenden Blaufärbung titriert.
Nachweis von Stärke mit Lugolscher Lösung:
1ml Iod-Lösung (0.150 g SZ, in 20 ml .

Iod, dann Rücktitration mit Thiosulfat-Lösung gegen Stärke . Hierzu wird die Zeit gemessen, die vom zusammengeben der Lösungen bis zu deren .Das Wichtigste auf einen Blick: Die Auswertung einer Titration erfolgt in fünf Schritten: Reaktionsgleichung aufstellen. Ich denke: I3- + H2O2 + 2H2O -> I3- + O2 + 2H3O+ .Für den Nachweis brauchen wir folgende Materialien: Wasser ; Salpetersäure (HNO 3) Silbernitrat (AgNO 3) Ammoniak (NH 3) Die Salzproben werden erstmal in verschiedene Reagenzgläsern aufgelöst, da alle Natriumsalze (Natriumchlorid, Natriumbromid & Natriumiodid) wasserlöslich sind. Es entsteht Iodstärke, die – je nach . Wässrige Lösungen von Thiosulfaten sind im basischen stabil. Bei Stärke denkt man in erster Linie an starke Menschen mit starken Muskeln. 1 Übermittelte Titrationskurve.
Experimente
) Rüdiger Blume.

Der Test gelingt mit Brot, mit Rüben oder oder mit aufgeschnittenen Kartoffeln. umgekehrt, also auf folgender Gleichgewichtsreaktion: 2 I − ⇌ I 2 + 2 e −.Wässrige Lösungen von Thiosulfaten sind im basischen stabil.Stärkenachweis (allgemein) Biologie-Wissen. In Anwesenheit von Stärke kommt es zu . Teilversuch b) Bei der Zugabe von Kaliumiodid färbt sich die Lösung dunkel blau. Äquivalenzpunkt identifizieren. Lehrerversuch – Bestimmung der Iodzahl Natriumthiosulfatlösung bis zur Entfärbung hinzutitriert und bei der Probelösung .

Die Iodometrie ist eine chemische Analysemethode, die zur quantitativen Bestimmung von verschiedenen Substanzen genutzt wird. Weitere Tipps des Monats. Die Reaktion ist ein chemisches Gleichgewicht.67 mg C13H16N3NaO4S . Es ist also eindeutig Stärke in eurem Brot vorhanden.Schritt: Thiosulfat wird durch Silberionen schnell ausgefällt, es entsteht sofort weißes Silberthiosulfat.

Beim Stärkenachweis tritt eine Blau- oder Violettfärbung auf.Nach Zugabe von Stärke wird die Lösung schwarz und entfärbt sich bei weiterer Titration mit Natriumthiosulfatlösung.Der Stärkenachweis dient zum Nachweis von Vielfachzuckern und Stärke.
Der Salzsäure-Thiosulfat-Versuch
Wir kochen eine Blaue Kartoffel und schneiden sie auf.Nachweise für Anionen nennt man chemische Reaktionen, mit denen ein Anion oder mehrere Anionen in einer Untersuchungssubstanz (Probe) nachgewiesen werden können. Experimente: Versuch: Temperaturabhängigkeit der Bildung des Iod/Stärke-Komplexes.
Stärkenachweis (allgemein)
NACHWEIS VON STÄRKE IN LEBENSMITTELN. Amylose kann man sich als kettenförmiges Molekül vorstellen, in dem viele Glucose-Ringe miteinander verknüpft . Chemische Reaktionen beruhen stets auf einem Donator-Akzeptor-Prinzip.Einstellung der DCPIP-Maßlösung: Mit der Vollpipette werden 25 ml Vitamin C-Lösung (entspricht 2,5 mg Vitamin C) sowie 2 Tropfen Essigsäure in ein kleines Becherglas gegeben und mit DCPIP-Lösung bis zur bleibenden schwachen Rosafärbung titriert.
Stärke löslich
Nernstsche Gleichung: [ ]
Chemikalien Iod (Xn), Kaliumiodid, destilliertes Wasser.
Nachweisreaktionen für Aldehyde und Ketone
Nachweis von Nährstoffen – Zusammenfassung. Du hast nun einige Methoden kennengelernt, mit denen man Zucker, Eiweiß und Fett in Lebensmitteln nachweisen kann.Aus diesem Grund wird die Landolt-Reaktion auch Landoltsche . alle Testsubstanzen, die bei Zugabe der Lugol-Lösung blau werden, enthalten Stärke.Ihre Salze enthalten das Thiosulfat-Anion S 2 O 3 2−. Keine Triiodide . Diese Seite ist Teil eines großen Webseitenangebots mit weiteren Texten und Experimentiervorschriften auf Prof. Sie ist zu unterscheiden von der Iodatometrie .Nachweise der Anionen. Die Bildung des Komplexes verläuft exotherm.

In diesem Video erkläre ich Euch, warum sich Stärke bei Zugabe von Lugolscher Lösung schwarzviolett verfärbt. (-> Reaktionsgleichung V05b .Trifft unsere Jodlösung auf die Stärke im Brot, gibt es eine chemische Reaktion, die dafür sorgt, dass sich das Gemisch blau färbt. Und wieder entfärbt es sich. In der Blindprobe werden 23,4 mL Abbildung 1: Die Titration von Natriumthiosulfatlösung zu der Probelösung.
Iodometrie
Heute im Chemieunterricht: | Liste von Nachweisreaktionen . Mittelwert Verbrauchte DCPIP in ml. (Farbänderung hatten wir nicht . Als Reaktionspartner dient entweder Iod (I2) oder Iodid, das während der Reaktion jeweils in die korrespondierende Redox-Form überführt wird: I2 + 2 e – ⇌ 2 I–.
Stärkenachweis
Die folgende Tabelle fasst die Nachweisreaktionen von Kohlenhydraten, wie Glucose und Stärke, von Eiweiß und von Fetten zusammen.Im Stoffwechsel unseres Körpers wird Stärke zu Zucker abgebaut, der zusammen mit den Fetten durch Veratmung (=Verbrennung) die Energie liefert, die der menschliche Organismus benötigt. In den Polyiodidketten ist die negative Ladung des Iodids über die gesamte Kette delokalisiert und die Elektronensysteme lassen sich leicht durch sichtbares Licht anregen, 0 3 . November 2015 Biochemie, Experimente, Nachweis, Schulversuch 0 Kommentare. Kaliumbromat-Maßlösung -Urtitersubstanz, Lösung ist gut haltbar, titerbeständig -wird 3 h bei 180 °C getrocknet -Reinheitsprüfung: 5 mL Bromatlösung mit 2 mL Schwefelsäure ( 2 mol L-1) ansäuern und 1 Tropfen 0. Bei höheren Konzentrationen erscheint die Färbung schwarz.Die bekanntesten Nachweisreaktionen für Aldehyde und Ketone sind die Tollens-Probe (auch Silberspiegelprobe), die Fehling-Probe, die Benedict-Probe, die Schiffsche-Probe sowie die Seliwanow-Probe. Du hast das vielleicht schon mal in Zusammenhang mit Ernährung gehört. Teilversuch c) Bei der Zugabe von Ammoniumthiocyanat zur Eisen (III)-Chlorid-Lösung färbt sich diese tief rot.7 Körper und Gesundheit Thema Verdauung und Ernährung – den Nährstoffen auf der Spur Basiskonzept Konzept der Wechselwirkung Kompetenzen/ Niveaustufen 2. Die Intensität der Farbe sagt etwas über den Anteil der . umgekehrt, also auf folgender Gleichgewichtsreaktion : Mit der Iodometrie . Phenazon-Gehaltsbestimmung EuAB (97): 0. 1) nachweisen, ob ein bestimmter Stoff auf molekularer Ebene eine Aldehyd . Bei diesem Versuch soll die Temperaturabhängigkeit der Reaktionsgeschwindigkeit erarbeitet werden.Voraussetzungen: Die SuS sollten den Nachweis von C-C-Doppelbindungen mit Bromwasser (V2) und den Iod-Stärkenachweis kennen. Die einfache Erklärung: Es ist keine . Diese sind für manche Stoffklassen ebenso unspezifisch wie für andere organische Verbindungen. Durchführung 1 g Iod und 2 g Kaliumiodid werden in etwa 4 ml destilliertem Wasser gelöst .Stärkenachweis – 4 Experimente zum Nachweis von Stärke in Lebensmitteln. Sie muss unbedingt abkühlen. Dagegen funktionieren andere Nachweise nur mit den gesuchten Verbindungen wie Stärke (siehe .Nachweis von Stärke mit Lugol-Lösung: Lugols Lösung enthält Jod.Dennoch sollte ihr ihn nur als zusätzliche Absicherung nach der Wassertropfenprobe verwenden. Bestimmung der Temperaturabhängigkeit der Geschwindigkeitskonstanten Arrheniussche Beziehung beschreibt die Temperaturabhängigkeit der Geschwindigkeitskonstante k: =?∙?− ?? ∙ (6) Hier ist ? Eine Iod-Kaliumiodid-Lösung (lugolsche Lösung) wird auf eine stärkehaltige Probe aufgetragen. In Gegenwart von Säuren zerfallen sie aufgrund der Unbeständigkeit der freien Thioschwefelsäure in einer Redoxreaktion . Der wechselseitige Nachweis von Iod und löslicher Stärke (Amylose) beruht auf der Bildung einer tiefblauen Einschlussverbindung, dem so genannten Iod-Stärke-Komplex.
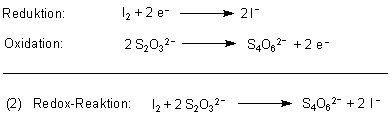
Beim Erwärmen verschiebt sich das Gleichgewicht auf die Seite der Edukte, da laut Le Chatelier durch die Erwärmung . Zur Durchführung wird die zu untersuchende Lösung mit einem Überschuss an Iodidionen versetzt. Sodaauszug für die Anionen, deren Nachweis durch Metallionen gestört wird. Im Labor kannst du durch verschiedene Farbreaktionen (z. Es liegt folgendes Gleichgewicht vor: Iod + Stärke ⇄ Tod-Stärke-Komplex + Energie. Stöchiometrische Berechnung der unbekannten Stoffmenge oder Stoffmengenkonzentration. er ist lange nicht so präzise wie die üblichen Tüpfelprobe mit Iod-Kaliumiodid-Lösung, dafür aber einfach, . Jod (Jod ist ein chemisches Element mit dem Symbol I und der Ordnungszahl 53) reagiert mit Stärke zu einer bläulichen Lösung, d. Bei uns bildete sich Gas. Zum Teil können diese Reaktionen auch für quantitative Bestimmungen eingesetzt werden. Aber Stärke kann auch andere Bedeutungen haben. Während der Titration darf die Temperatur der Lösung 10°C nicht übersteigen. Das in Chemie und Technik wichtigste Thiosulfat ist das Natriumsalz und Ammoniumsalz, auch Fixiersalz . Es gibt Anionennachweise, bei denen Anionen wie Carbonat, Sulfid und Acetat direkt aus der Probe nachgewiesen werden können, und weitere Anionennachweise, die nur aus . Als alleiniger Silicat-Nachweis erscheint er uns zu dürftig und fehleranfällig. Die Iodometrie ist ein analytisches, titrimetrisches Verfahren zur quantitativen Bestimmung von oxidierenden Substanzen für die kein geeigneter Indikator zu Verfügung steht. Bestimmung reduzierender .info Experimente 22.Erklärung [ Bearbeiten] 1.Iodometrie – Eine Maßanalyse mit Stärke! C3CL ⭳ : laborberufe. Dabei wird meistens eine Iod-Kaliumiodid-Lösung ( Lugolsche Lösung) eingesetzt, die auf eine feste Probe geträufelt oder mit einer Probelösung versetzt wird. Materialien: Reagenzglasständer, 2 Reagenzgläser, 2 Gummistopfen, 4 Bechergläser (100 ml), Uhrglas, Spatel Chemikalien: Palmin, Speiseöl, Stärke, Lugol-Lösung, essigsaures Wasser
Nachweisreaktionen organischer Naturstoffe
Die Iodometrie ist eine chemische Analysemethode, die zur quantitativen Bestimmung von verschiedenen Substanzen genutzt wird. Natürliche Stärke ist ein Stoffgemisch zweier Vielfachzucker: Amylose und Amylopektin.Beim Erhitzen (Schutzbrille!) färbt sich die Lösung aufgrund der Bildung von Permanganat-Ionen purpurfarben.1 % Methylorange dazu, rosa Farbe darf nach 2 min nicht verschwunden sein . Sobald die Salzsäure im Kolben ist, stellt man diesen auf ein weißes Blatt Papier, auf dem sich ein schwarzes Zeichen befindet.de Reduzierende oder oxidierende Analyte lassen sich iodometrisch bestimmen. Bei diesem Versuch handelt es sich lediglich um einen Geschmackstest, d.
6 Redoxreaktionen
Eine relative Bekanntheit erlangte diese Reaktion, weil unter bestimmten Bedingungen die Blaufärbung nicht schlagartig auftritt, sondern erst nach einer längeren Zeitphase nach dem Mischen der Edukte. Stärke lässt sich mit Hilfe der Lugolschen Lösung (Jod-Jodid-Lösung) durch eine intensive Blaufärbung nachweisen. Aus salpetersaurer Lösung fallen sie als dicker („käsiger“) weißer (Chlorid) bzw.
Nachweise
Zuerst sieht man nichts. Man gibt dann etwas . Ergebnis: Die Iod-Stärke-Reaktion ist positiv und überdeckt das natürliche Blaulila der Knolle. In der Komplexchemie fungieren die Liganden als Donatoren, indem sie Elektronen für eine koordinative Bindung zur Verfügung stellen.Die Iod-Stärke-Reaktion dient zum Nachweis von Iod bzw.
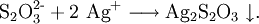
Iod bildet mit dem Amylose-Anteil der Stärke eine dunkelblaue Einschlussverbindung. Stoffmengenverhältnis ermitteln. ??♀️
Brom(at)ometrie
Polyiodid +Stärke ⇌Polyiodid−Stärke−Komplex Die Ketten können gut in die Stärke-Helix eingebaut werden und interagie-ren mit den Hydroxygruppen der Zuckermoleküle. Bei der Zugabe der Salzlösung, entfärbt sich diese.Der Iod-Stärke-Komplex. Dabei wird ein Iod-Stärke-Komplex gebildet, der durch Einlagerung der Iodmoleküle in die Helixstruktur der Stärke zu einer blauen Färbung führt. Man gibt Natriumsulfit hinzu. Bei diesen Experimenten geht es um das Kohlenhydrat Stärke. Trifft die Jodlösung auf den Brotklumpen, den ihr im Mund eine Weile zu Brei zerkaut habt, färbt sich nichts blau. Dann tropfen wir etwas Iod-Iodkalium-Lösung (Lugolsche Lösung) auf die Schnittfläche.05 mol/l) = 16. gelblicher (Bromid, Iodid) Niederschlag aus. Lugolscher Lösungfolgende Fragen/Aspekte werden geklärt:- Vorhandensein von Stärke in pflanzlich. Dabei werden Iodatome unter Bildung einer blauen Farbe in das Stärkegerüst eingebaut.Thiosulfate sind Derivate der im freien Zustand unbeständigen Thioschwefelsäure H 2 S 2 O 3. Die Iodprobe (Iod-Stärke-Reaktion) ist ein chemisches Verfahren zum Nachweis von Stärke mit Hilfe einer Iod -haltigen Lösung.Mit Lugolscher Lösung lässt sich Stärke nachweisen. In Gegenwart von Säuren zerfallen sie aufgrund der Unbeständigkeit der freien Thioschwefelsäure in einer Redoxreaktion langsam zu Schwefel, Schwefeldioxid und Wasser: . Teilversuch a) Es fällt ein weißer Niederschlag aus. EINORDNUNG IN DEN RAHMENLEHRPLAN Themenfeld 3. Reload – diesmal mit Laserpointer. aus dem Sodaauszug (Sodaaufschluss) Aus Ursubstanz: Carbonat, Nitrat, Acetat, da sie sich im Laufe der Analyse verflüchtigen können; Sulfid.Man benutzt die vorherige Iod Stärke Lösung (die man mit KI-Lösung gemischt hat) Und gibt dazu ein paar Tropfen H2O2.Der Thiosulfat-Nachweis kann nur durch Sulfid gestört werden, welches in Gegenwart von Silberionen sofort als Silbersulfid ausfällt. So werden bei den Säure-Base-Reaktionen von den Säuren Protonen abgegeben und von den Basen diese aufgenommen. Nachweisreaktionen sind möglichst spezifische chemische Reaktionen, die qualitativ das Vorhandensein eines Ions oder einer Stoffgruppe anzeigen und mit einfachen Mitteln durchgeführt werden können. Zu beachten ist, dass Fluorid -Ionen, die ja auch unter die Halogenid-Ionen zählen, keinen Niederschlag .1 Dinge/Lebewesen beeinflussen sich gegenseitig 2.Iod-Kaliumiodid-Probe. [1] Sie gehört zu den titrimetrischen Analyseverfahren und beruht auf der Umwandlung von Iodid-Ionen (I −) in Iod (I 2) bzw. Nun startet man eine Stoppuhr und misst die Zeit, die vergeht, bis man das schwarze .
Aus Ursubstanz bzw. Warum ist bekannt. Erst dann gibt man die Salzsäure dazu.6 Redoxreaktionen. Da die Bildung des .Schulen sind solche Methoden jedoch kaum verfügbar und man greift deshalb immer noch auf die klassischen Nachweisreaktionen der Naturstoffe zurück.Versuch 1: Iod-Stärke-Reaktion mit der Blauen Kartoffel. Zuerst werden das Thiosulfat und das Wasser in die Kolben gegeben. V 3 – Die Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur: Die Reaktion von Salzsäure mit Natriumthiosulfat bei verschiedenen Temperaturen. Erklärung der Durchführung der Silicat-Nachweise, inklusive Schemata und Video der Versuche, sowie einer Auflistung häufiger Fehler und Störungen.Nachweisreaktion von Stärke/Amylose mit Iod-Kaliumiodid bzw.Die Silbersalze der Halogenide Chlorid, Bromid und Iodid zeichnen sich durch ihre Schwerlöslichkeit aus.Bei Zugabe von Stärke führt das entstehende Iod zu einer Blaufärbung der Lösung (). Tropft man Iod-Kaliumiodid-Lösung auf ein stärkehaltiges Nahrungsmittel, erfolgt eine Blau- oder Violettfärbung, die auf Stärke hinweist. Es blieb dunkelblau trüb). Geräte Becherglas (200 ml), Rührstab aus Glas. [1] Sie gehört zu den titrimetrischen Analyseverfahren, und beruht auf der Umwandlung von Iodid-Ionen (I –) in Iod (I 2) bzw.viel schneller als die Oxidation von Iodid verläuft und es dabei eine Iod/Stärke Komplex gebildet wird. Um diese Störung zu umgehen, kann das vorhandene Sulfid zuerst durch Hinzugabe von . Nachzuweisender Nährstoff.
Thiosulfate
- Thermovorhang Für Haustüren , Thermo Türvorhänge online kaufen
- Thyrotoxicosis Treatment Guidelines
- Thermische Druckgebilde Definition
- Thumbnail Programm Kostenlos | KI Thumbnail-Creator
- Thomaduo Kombipräparat | Premium Vitamin D3+K2 Tropfen
- Thermischer Glasbruch Wer Zahlt Was
- Thermacare Schmerzgel Anwendung
- Theorem Der Axiomatisch – Axiomatische Mengenlehre
- Thomann In Der Nähe : Das Riemann-Thomann-Modell [+ Tipps für Teamleitung]
- Therapeutische Unterstützung Messie