Stoffmengenanteil Formel : Stoffmenge
Di: Samuel
einsetzen und erhältst den Partialdruck und somit den Dampfdruck von Sauerstoff und Stickstoff.Schließ dich über 22 Millionen Schülern und Studierenden an und lerne mit unserer StudySmarter App! Die erste Lern-App, die wirklich alles bietet, was du brauchst, um deine Prüfungen an einem Ort zu meistern.
Raoultsches Gesetz
Lösungen, Stoffmengen und Konzentrationen
Der Massenanteil ist gemäß DIN 1310 eine Gehaltsgröße (auch Gehaltsangabe genannt), .So berechnest du die Stoffmenge – Mol-in-Gramm-Umrechner. Möglich, aber weniger üblich ist, den Gehalt . Stoffmenge: Wasserstoff Berechnen Formel Einheit Definition StudySmarter Original!
Stoffmengenanteil (Chemie)
Das Zerfallsgesetz beschreibt den Zerfall instabiler Kerne: In eine bestimmten Zeit (Halbwertszeit) zerfällt jeweils die Hälfte der vorhandenen Kerne.Der Masseanteil sagt dir den Prozentanteil von jedem der Elemente, die eine chemische Verbindung bilden. Früher wurde Massenanteil auch bezeichnet als Massenbruch.Für Lösungen ist die gebräuchlichste Zusammensetzungsgröße die Stoffmengenkonzentration, weil aus dieser Größe die Stoffmenge eines gelösten Stoffs direkt aus dem Volumen der Lösung ermittelt werden kann. (Weitergeleitet von Stoffkonzentration) Die Stoffmengenkonzentration ( Formelzeichen: c) oder Molarität (veraltete Bezeichnung) ist der Quotient aus der Stoffmenge ( n) eines gelösten Stoffes X und dem Volumen ( V) der Lösung. eine Summe in Excel berechnen Damit Du schnell und effizient eine Summe in Microsoft Excel berechnen kannst, bietet Microsoft hierfür.Stoffmengenanteil Wasserstoff = n(H 2) : [n .
4 Wege um die Molarität (Stoffmengenkonzentration) zu berechnen
Weg 1: Denke dir einen Zwischenschritt. Durch die Angabe der .Bei dieser Reaktionsgleichung ist es leicht nachzuvollziehen, wie die Stoffmengenverhältnisse sind. Stoffmengenanteil : Stoffmengenanteil des gelösten Bestandteils/Summe der Stoffmengen aller Bestandteile; z.Der Stoffmengenanteil ( Molenbruch ) des gelösten Stoffes ist das Verhältnis der Anzahl der Mole gelösten Stoffes zur Anzahl der Mole der Lösung (Lösungsmittel + gelöster Stoff). Berechnen Sie anhand des tabellierten Atomgewichts von Kupfer (M = . Setzen wir nun diese Zahlen in die obige Gleichung ein: Stoffmenge = 10 / 36,5 = 0,27 Mol = 1,626·10²³ .Eine Berechnung mit Mathematische Formeln, wie z. Diese findest du meist in Tabellen am Ende von . \text {1 mol} 1 mol besteht aus 600.Der Stoffmengenanteil der schwarzen Kugeln ist 10 pro 40, als Bruch 10/40 oder kurz 1/4 oder 0,25 oder 25 %. Du kannst entweder die Gesamtmenge der Substanz erhöhen (gib z. Chemische Größe. Wenn man sich diese Formeln nun betrachtet, könnte man meinen, dass die Größen “Volumenanteil” und “Volumenkonzentration” das Gleiche sind.Mit dieser Berechnung beschäftigen wir uns hier. Im Stoffgemisch einer Lösung tritt der Lösungseffekt auf. Für die Volumenkonzentration eines gelösten . Kennzahl (Chemie) Die Volumenkonzentration ( Formelzeichen: σ) ist eine Gehaltsangabe für Mischphasen, zumeist von Lösungen. Physikalische Chemie.
Es gibt 2 Wege, den Anteil zu bestimmen. Ein Mol entspricht einer Anzahl von . Die Stoffmenge ist also der Quotient aus Masse und molarer Masse eines Stoffes. Siehe auch ppm ↗ Formelzeichen. Nun wird das eine entfernt (feuchte Luft und das Wasser mit einen Stoffmengenanteil von 2% wird entfernt). Mit ihr gelten für reale Mischungen die gleichen Gesetzmäßigkeiten (bezüglich physikalischer Messparameter wie Gefrier-, Siedetemperatur, Leitfähigkeit von Elektrolytlösungen, . Prozent abziehen: 50 % von 100 sind 50. Denke dir einen Zwischenschritt.
Aktivität (Chemie)
Zur Erinnerung: Die Formel, um die molare Masse berechnen zu können, lautet: M = m / n. ( Zustandsgröße ).Die in vorstehender Tabelle in den Gleichungen beim Stoffmengenanteil x und Teilchenzahlanteil X auftretenden Nenner-Terme sind gleich der mittleren molaren Masse des Stoffgemisches und können entsprechend ersetzt werden: . Wenn du das weißt, kannst du in einem Experiment beispielsweise die Masse eines Stoffes ermitteln. Lass uns anhand eines kurzen Beispiels erklären, wie man Mol in Gramm oder Gramm in Mol umrechnet. Die Konzentration gibt den Anteil eines gelösten Stoffs in einer definierten Lösungsmenge an. Den Masseanteil zu finden erfordert die Molmasse der Elemente in der Verbindung in Gramm/Mol oder die Anzahl an Gramm, die verwendet wurden, um die Lösung herzustellen.Die Gehaltsangaben von Lösungen (Gehaltsgrößen ) lassen sich auch folgendermaßen wiedergeben: Massenanteil : Masse des gelösten Bestandteils/Masse der Lösung; z.
Raoultsches
Die Stoffmengenkonzentration wird in der Einheit mol/l angegeben. Wenn ich also das Stoffmengenverhältnis aufstelle, sieht es so aus: n(C) = n(O 2) = n(CO 2) Wenn wir 1 mol Kohlenstoff in die Reaktion hineingeben, .
Zerfallsgesetz und Halbwertszeit
Gehaltsangaben – auch Gehaltsgrößen genannt – geben in Chemie und Physik den Gehalt eines Stoffes in einem Stoffgemisch an ( DIN 1310 ), [1] quantifizieren also den materiellen Anteil eines einzelnen Stoffes an einem festen, flüssigen oder gasförmigen Gemisch, beispielsweise einer wässerigen Lösung oder einer Legierung . Die molare Masse des . Die Stoffmenge wird in mol angegeben. Die Stoffmengenkonzentration ist eine Größe, die Lösungen charakterisiert. Sie werden durch eine einfache Formel berechnet, in der die . Berechnet wird er über den Bruch mit dem Volumen der Komponente als Zähler und der Summe der Volumina aller .Die Formel zu Berechnung der Stoffmenge lautet: n = m : M (Stoffmenge n ist der Quotient aus Masse m und molarer Masse M. Die Stoffmenge gibt die Teilchenanzahl einer Stoffportion an. Multipliziert man den Massenanteil mit 100 %, so lässt er . Allgemein ist der Volumenanteil oder Volumenbruch ( Formelzeichen: υ, häufig auch φ) einer Komponente in einem Stoffgemisch das anteilige Volumen der Komponente an der Summe der Volumina aller Komponenten. Der Gesamtdruck setzt sich additiv aus den Partialdrücken der einzelnen Gaskomponenten zusammen. Diese Stoffmenge ist dabei weder Masse, noch Teilchenzahl, sondern im Internationalen Einheitensystem (SI) durch willkürliche Vereinbarung als Basisgröße eigener Art festgelegt. Jetzt ist die Frage, wie sich der Stoffmengenanteil der anderen verändert.Es gilt: n = \dfrac {m} {M} n = M m.Auf sie greifst du bei den meisten Dampfdruck-Aufgaben zurück, auf die du in der Physik oder Chemie stößt. Der Unterschied liegt darin: In die . Dadurch musst du nur noch beide Zahlen in die Formel. Auch 100 % von oder auf 100 sind ganz klar: Prozent aufschlagen: 100 % auf 100 sind 200. Eine Stoffportion besteht aus einer unvorstellbar großen Anzahl an Teilchen. Damit Du nun den Prozentualen Wert berechnen kannst, . Das Mischen von Lösungen unterschiedlicher Konzentrationen oder das Verdünnen hoch konzentrierter Lösungen sind alltägliche Aufgaben z. Sie gehört zu den Gehaltsangaben und ist definiert als der Quotient aus dem Volumen einer Komponente und dem Gesamtvolumen der Mischphase.Entsprechend bekommst du folgendermaßen den Stoffmengenanteil für Sauerstoff: Die Gleichgewichtsdampfdrücke und hast du meistens angegeben.Stoffmengenkonzentration – Definition. Beträgt der Massenanteil 1 liegt die entsprechende Komponente in Reinform vor, beträgt er 0, ist sie nicht im Gemisch enthalten.
Dampfdruck • einfach erklärt: Definition, Berechnung
Stoffmengenkonzentration. Wenn wir wissen, dass Lithium eine molare Masse von M(Li) = 6,94 g/mol besitzt, heißt das, dass 1 mol Lithium 6,94 g wiegen.
Partialdruck
Irgendwann nimmst du bestimmt nur den 2. Die Abkürzung für die Stoffmengenkonzentration ist c. Die Stoffmenge und Masse eines Stoffes lassen sich also über die molare Masse ineinander umrechnen. Lösung: Setze nun die gegebenen Werte für die Masse und die Stoffmenge in die Gleichung ein. Antwort: Die Halbwertszeit beträgt 2,06 Stunden. Nehmen wir an, wir wollen 2 mol Lithium und 2 mol Blei.Der Massenanteil ist somit ein Maß für die anteilige Masse einer Komponente an einem Gemisch und findet vor allem in T-w- Phasendiagrammen Verwendung. Dann multiplizierst du die Stoffmengenkonzentration der Säure mit dem Volumen der Säure – 1,25 ∙ 35 = 43,75 und dividierst das Ergebnis durch das Volumen der Base. Verringern (gib z. Dabei muss man schnell berechnen können, welche Konzentrationen die erhaltene Lösung besitzt oder welche . Der Gehalt des gelösten Stoffs kann aber auch als Massenanteil oder Massenkonzentration angegeben werden.Hierfür gibt es auch eine einfache Formel, aber intuitiv kommt man bereits weit. Du willst vom Ganzen (100 g) zum Bruchteil (40 g) kommen. Eine Stoffportion kann durch die physikalische Größe Stoffmenge gekennzeichnet werden.

0,5, 1/2 oder 3/4 . Das bedeutet, sie ist auch nicht durch andere SI-Basisgrößen . Die molare Masse der Elemente des Stoffes findest du mithilfe des . Wie das geht, sehen wir uns im Folgenden an.
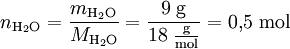
[1] Bei Kenntnis der molaren Masse lässt sich aus der Stoffmengenkonzentration die .Übersicht der Formeln zur Berechnung der Stoffmenge.
Massenanteil
in der chemischen Analytik oder in der chemischen Industrie. Außerdem gehen wir auf die Bedeutung der Stoffmengenkonzentration ein.Du kannst unser Tool auch als 5 zu 1 Mischungsverhältnis-Rechner verwenden – klicke auf den Button Erweiterter Modus und gib den Wert ein, um den du die Mengen deiner Stoffe verändern möchtest.Auf beiden Seiten des Diagramms enden die idealen und die realen Kurven in denselben Punkten. – Wie bestimmen die Stoffmenge n der abgewogenen Masse: n = m : M = 73 g : 36,5 . Wir wissen, dass wir 10 g HCl haben, mit einer Molekülmasse von 36,5 g/Mol. Die Molarität drückt die Beziehung zwischen der Stoffmenge eines gelösten Stoffes pro Liter einer Lösung, oder das Volumen dieser Lösung aus.Sichere dir jetzt die perfekte Prüfungsvorbereitung! In diesem Online-Kurs zum Thema Stoffmenge, Molare Masse, Konzentration wird dir in anschaulichen Lernvideos, leicht verständlichen Lerntexten, interaktiven Übungsaufgaben und druckbaren Abbildungen das umfassende Wissen vermittelt.

Letztere ist die Summe der Stoffmengen aller Komponenten ( i mit . 1 cg g −1 = 1 %. Man unterscheidet zwischen extensiven und intensiven Z. Die relative Erniedrigung des Sättigungsdampfdrucks über der Lösung mit ebener Oberfläche (Krümmungseffekt) ist dabei gleich dem Produkt aus dem Dampfdruck des Lösungsmittels mal seinem Stoffmengenanteil. Auch wenn also eine Substanz dem . 1 mol mol −1.Der Stoffmengenanteil x i ist definiert als Wert des Quotienten aus der Stoffmenge n i der betrachteten Mischungskomponente i und der Gesamtstoffmenge n des Gemisches. In der Formelschreibweise kann die Molarität wie folgt ausgedrück werden: Molarität = Stoffmenge einer Lösung / Liter einer LösungStoffmengenkonzentration – Formel und Einheit. Wenn wir 2 mol wollen, müssen wir also 2 mol * 6,94 g/mol = 13,88 g Lithium . Sie gibt an, wie viele Teilchen (einer bestimmten Teilchensorte, etwa Natriumkationen oder Kohlenstoffdioxidmoleküle) pro Liter der entsprechenden Lösung vorliegen.
Konzentrationen: Molalität und Stoffmengenanteil ( Molenbruch )
Mit Stoffmenge wird die quantitative Mengenangabe für Stoffe, besonders in der Chemie, bezeichnet.
Gehaltsangabe
2, 4 oder 6 ein), oder.Kenne die Formel zur Berechnung der Molarität. Gegeben sei eine verdünnte wässrige Lösung von Schwefelsäure H 2 . Es gibt das Verhältnis der Stoffmengen zweier betrachteter Mischungskomponenten zueinander an.Ein Rechner für Menge und Prozent einer Mischung aus verschiedenen Stoffen. Allerdings sind Volumenanteil und Volumenkonzentration zwei verschiedene Größen.
Stoffmenge
Die Gleichung sieht wie folgt aus: ln (P1/P2) = (ΔHvap/R) ( (1/T2) – (1/T1)). Als Formelzeichen verwendet werden w, gelegentlich auch ω, y oder ξ. Jetzt weiter lernen! Die Menge kann eine Angabe wie Masse, Gewicht, Volumen oder Stückzahl sein, die Prozent beziehen sich dann auf diese Größe.Partialdruck bezeichnet den Teildruck einer einzelnen Komponente oder Fraktion in einem Gasgemisch.Die betreffende physikalische Größe wird als Teilchenanzahl bezeichnet. Weg, denn er ist schneller.Einsetzen der Werte ergibt für die Halbwertszeit.
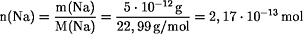
Ich habe vier Komponenten angegeben und der Stoffmengenanteil in der Luft. Der Partialdruck entspricht dem Druck, den die einzelne Gaskomponente bei alleinigem . Bei 50 % von oder auf 100 ist es ganz einfach, das bekommt jeder noch hin: Prozent aufschlagen: 50 % auf 100 sind 150.Bestimmen Sie die stöchiometrischen Koeffizienten a bis d in folgender Formel: a SiO 2 ∙b Al 2 O 3 ∙c CaO ∙d H 2 O (5 SiO 2 ∙2 Al 2 O 3 ∙3 CaO ∙4 H 2 O) (7) Bei den beiden natürlich vorkommenden Kupferisotopen handelt es sich um 63Cu (M = 62,9298 g/mol) und 65Cu (M = 64,9278 g/mol). Beispiel: – Wir wiegen eine Masse m = 73 g Wasserstoffchlorid (HCl) ab.Raoultsches Gesetz der Dampfdruckerniedrigung.Aktivität (Chemie) Die Aktivität ist eine thermodynamische Größe, die in der physikalischen Chemie anstelle der Stoffkonzentration verwendet wird. Sie werden gemacht in Bezug auf die Größen: Stoffmenge n. Rechenbeispiele Verdünnte Schwefelsäure. ppm als Stoffmengenanteil Die Einheit ppm als parts per million gibt zum Beispiel die Stoffmenge von CO2 in der Atmosphäre als Anteil der gesamten Anzahl von Teilchen an.
Mischungsverhältnis Rechner
Bis zu fünf Stoffe können eingegeben werden.
Teilchenanzahl und Stoffmenge in Physik
Die in Mol gemessene Stoffmenge gibt an, das Wievielfache einer bestimmten Teilchenanzahl in einer Stoffportion verliegt. Bitte von einem Stoff Menge und Prozent angeben, von den anderen Stoffen einen dieser beiden .Mischungsrechnen. Die Stoffmenge steht zur Teilchenanzahl, Masse und zum Volumen in jeweils einer bestimmten Abhängigkeit. Klingt einfacher als es irgendwie ist, ich komme nicht auf die gegebene . 1 Teilchen Kohlenstoff reagiert mit einem Teilchen Sauerstoff zu einem Teilchen CO 2.
Stoffmenge einfach erklärt
Stoffmenge: Berechnen, Einheit & Formelzeichen
Die molare Masse M von Wasserstoffchlorid ist 36,5 g/mol.Gehaltsangaben – auch Gehaltsgrößen genannt – geben in Chemie und Physik den Gehalt eines Stoffes in einem Stoffgemisch an, quantifizieren also einen materiellen Anteil eines Stoffes an einem Gemisch, beispielsweise einer Lösung.
Stoffmengenverhältnis aufstellen aus Reaktionsgleichung
Der Massenanteil gibt den relativen Anteil einer Masse an der Gesamtmasse eines betrachteten Stoffgemisches an.In diesem Fall kannst du die Formel für das Verhältnis von 1:1 verwenden, da ein Mol HCl mit einem Mol NaOH reagiert. Die Variablen in dieser Formel stehen für: ΔHvap: Die molare Verdampfungsenthalpie der Flüssigkeit. Die Stoffmengenkonzentration ( Formelzeichen: c) oder Molarität (veraltete Bezeichnung) ist der Quotient aus der Stoffmenge ( n) eines gelösten Stoffes X und dem Volumen ( V) der Lösung.

Addition, Subtraktion, Multiplikation und Division sind der Grundbaustein. Die Stoffmengenkonzentration der . Mit der Stoffmenge kann man sich diese Zahl besser vorstellen.Zusammensetzungsgrößen, Zusammensetzungsvariable, Gehaltsgrößen, früher Konzentrationsmaße, Größen, die die quantitative Zusammensetzung gasförmiger, flüssiger oder fester Mischungen (Mischphasen) beschreiben. Zum Beispiel, Xso = 0, 2 bedeutet 0, 8 mol Lösungsmittel sv enthalten 0, 2 mol des . Wie die Beobachtung zeigt, schmiegt sich die Kurve einer realen Substanz tangential an die ideale Raoultsche Gerade an, wenn der Stoffmengenanteil dieser Substanz sich dem Wert $ 1 $ nähert. Stoffmengenanteil ( Molenbruch ) des gelösten Stoffes: Xso = nso nso+nsv. Als Formelzeichen üblich ist ein . M = 130 g / 0,4 mol = 325 g/mol. A) Extensive Z. Die Summe aller Partialdrücke ergibt den Gesamtdruck. [1] Bei Kenntnis der molaren . 40 100 40 100 kannst du kürzen: 40 100 = 4 10 = 2 5 40 100 = 4 10 = 2 5.Das Stoffmengenverhältnis ( Formelzeichen: r) ist gemäß DIN 1310 eine sogenannte Gehaltsgröße, also eine physikalisch-chemische Größe zur quantitativen Beschreibung der Zusammensetzung von Stoffgemischen / Mischphasen.
- Strahlenexponierte Beruf , Dosimetrie und berufliche Strahlenexposition
- Strand Laguna Stella Maris _ Apartments Stella in Umag, Istrien, Kroatien
- Stirling Castle Scotland , Stirling Castle in Scotland
- Strandkorb Mit Rollen Eingebaut
- Stille Reserven Bilden Buchungssatz
- Strahlentherapie Hamburg Mörkenstraße
- Stoffschere Prym – Die besten Stoffscheren Prym
- Stimmrechtsübertragung Gmbh | Treuhand bei der GmbH: Besonderheiten beim Treuhandvertrag
- Stoffschuhe Reinigen Und Waschen
- Strandmuschel Verschließbar – Explorer Strandmuschel verschließbar
- Stihl Msa 160 C Ersatzteile | Stihl Akkumotorsägen MSA 160 C C