Punto Isoeléctrico Fórmula , Carga de las biomoléculas
Di: Samuel
El punto isoeléctrico de la alanina se da a pH 6,00. Cuando una proteína se encuentra a un pH diferente a su punto isoeléctrico . La ecuación de Henderson-Hasselbalch es una fórmula matemática utilizada para calcular, de manera muy rápida y sencilla, el pH aproximado de una disolución buffer, tampón, o amortiguadora del pH.Aula Virtual de Biología.Introduzca el péptido de una secuencia de las letras & #8212 ‚ASELP‘ en nuestro ejemplo & #8212 en el cuadro y haga clic en ‚Calcular. La histamina es una sustancia liberada por las células del sistema inmune durante una reacción alérgica.Formula general . El punto isoeléctrico (pI) es el pH para el cual una proteína presenta carga neta compensada (igual número de cargas positivas que negativas) y en el mismo, la solubilidad de la proteína es mínima.

En nuestro ejemplo, el pI es 4. Cosméticos: Se utiliza en productos como polvos faciales y máscaras de arcilla. La cisteína (abreviada como Cys o C) es un α-aminoácido con la fórmula química HS-CH 2-CHNH 2-COOH.El pH isoeléctrico se puede definir como el pH al que existe un aminoácido como un ion dipolar, es decir, como un ion híbrido con carga neta 0 y no tiene tendencia a migrar bajo la influencia de un campo eléctrico . Desde la distancia la nube se ve neutra.Si es necesario, consulte la tabla de conversión de tres letras a una letra que se proporciona en Recursos.Escriba la fórmula desarrollada del dipéptido glicil-histidina.Si el pH fuera 4, 7 el aminoácido tendría una carga positiva al estar en un medio acido, por lo tanto se desplazaría al cátodo. Los aminoácidos son compuestos sólidos; incoloros; cristalizables; de elevado punto de fusión (habitualmente por encima de los 200 ºC); solubles en agua; con actividad óptica y con un comportamiento anfótero.El punto isoeléctrico se define como el pH en el cual el número de cargas positivas se iguala al número de cargas negativas que aportan los grupos ionizables de una molécula.
Triptófano
En este punto, la proteína tiende a tener una menor solubilidad en agua debido a la disminución de las interacciones electrostáticas.340 g cm-3: Punto isoeléctrico: 5. tenga en cuenta que el servidor también calcula el peso molecular (mw) del péptido. Proteína transportadora del cobre.89 Número CAS: 73-22-3 Categorías: Aminoácidos esenciales | Aminoácidos neutros no polares | Triptaminas | Antidepresivos : Este articulo se basa en el articulo Triptófano publicado en la enciclopedia libre de Wikipedia. Vea también Hg2+ Estructura, características: 17 datos completos rápidos.El pH isoeléctrico, también conocido como punto isoeléctrico, es el pH en el cual una proteína tiene carga neta igual a cero.0: el único aminoácido que carece de carbono quiral: alanina: Ala (A) Ácido 2-aminopropanoico: 6. La caseína está formada por alpha(s1), alpha(s2)-caseína, ß-caseína, y kappa-caseína formando una micela o unidad soluble.
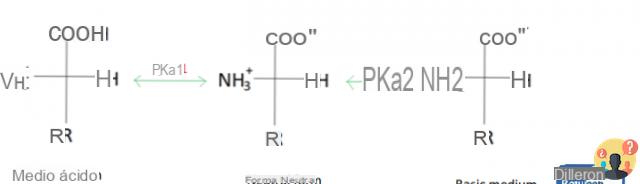
Moreno Salazar Material exclusivamente para uso educativo y no de lucro 73 En la figura anterior se muestra el efecto que tienen tanto el grupo carboxilo como el amino . valina amino estructura ácida a ph bajo. Verdadero, ya que los procesos de laboratorio imitan los procesos naturales.Determinación del punto isoeléctrico La determinación del punto isoeléctrico se llevó a cabo de acuerdo al método descrito por Spell y Bressani [32] modificado [31]. El pH particular al que existe un aminoácido dado en solución como un zwitterión se denomina punto isoeléctrico (pI). Propiedades de los aminoácidos.Este aminoácido tiene unas constantes de disociación pK 1 de 2. A este pH, la caseína se encuentra en su punto de menos solubilidad, debido a que hay menos repulsiones intermoleculares, por lo que precipita. Ceruloplasmina. La actividad óptica se manifiesta por la capacidad de desviar el .21 g mol-1: Punto de Fusión 281 °C Densidad 1. Desmitifiquemos juntos el proceso. Para aminoácidos con más de un grupo ionizable, por ejemplo, lisina o aspartato, se utiliza la misma fórmula.21, y un punto isoeléctrico de 5. El contenido está disponible bajo los . Ni la alfa ni la beta caseína son solubles en la leche, solas o combinadas.

Puede utilizar los valores de pK para los aminoácidos aislados, no obstante que cuando los aminoácidos se unen para formar péptidos y proteínas, los valores de pK de sus grupos ionizables, se ven afectados
Punto
La arginina es un amino básico (+ muy cargado) ácido que tiene un [.• Punto isoeléctrico: Es el P H en el que el aa tiene tantas cargas positivas como negativas. Depende de su estructura química, de qué grupos ionizables posea.
PAU BIOLOGIA PROTEINAS 2019

Funciones La metionina es un aminoácido esencial para la síntesis de muchas proteínas, entre las que están algunas hormonas, las proteínas constitutivas de la piel, pelo y uñas, etc. (c) ¿Qué son los aminoácidos esenciales? (0,5).Respecto a las proteínas: a) Dibuje la fórmula general de un aminoácido. (b) ¿Qué es el punto isoeléctrico de un aminoácido? (0,5).El punto Isoeléctrico (o pH isoeléctrico) de la caseína es 4.Fórmula química: C 5 H 11 NO 2 S Masa molar: 149. Embarcarse en el viaje de comprender el punto isoeléctrico abre puertas para desentrañar las complejidades de las moléculas.El punto isoeléctrico es el pH al que una sustancia anfótera tiene carga neta cero. Estos puntos isoeléctricos pueden afectar la solubilidad de las proteínas y su capacidad para . Formula el hexapéptido (Nt)Ala-Gly-Tyr-Glu-Val-Ser (Ct)
Cisteína
d) Solubilidad : Al ser dipolares son solubles en agua y su punto de fusión es elevado . A este pH, la caseína se encuentra en su punto de menor solubilidad, debido a la reducción de repulsiones intermoleculares, por lo que precipita.Fórmula estructural (a pH 6) Punto isoeléctrico (pI) Característica distintiva; Aminoácidos con un grupo R no polar: glicina: Gly (G) ácido aminoetanoico: 6.
Caolín
Además, la alanina aminotransferasa (ALT) . En nuestro ejemplo, el pI es de 4. Sus concentraciones pueden encontrarse elevadas durante procesos inflamatorios, cirrosis, leucemias agudas, enfermedad de Hodking y artritis reumatoide.
¿En qué consiste el punto isoeléctrico? ⁉️
FÓRMULA MOLECULAR: C3H7O2N MASA MOLECULAR: 89 g/mol PUNTO ISOELÉCTRICO: 6,00 Aminoácido neutro que forma parte del código genético Aminoácido no esencial que puede ser considerado esencial en ciertas circunstancias El carbono alfa tiene como sustituyente a un grupo metilo levo-rotatorio, lo cual lo hace uno de los . Las proteínas tienen diferentes puntos isoeléctricos dependiendo de su composición de aminoácidos. Si una molécula o una parte de ella resiste el contacto con la molécula de agua, entonces la naturaleza se llama hidrofóbico naturaleza. Algunos de los usos más comunes incluyen: Fabricación de papel: Mejora la impresión y la opacidad del papel. Punto isoeléctrico de . Otra definición de punto isoelectrico es: pH al que la concentración de especies protonadas y desprotonadas se iguala. Continuar Leyendo >. Ingrese la secuencia de una letra del péptido (ASELP en nuestro ejemplo) en el cuadro y haga clic en Calcular. Leer el punto isoeléctrico (pI) valor dado en la línea de ‚Teórico pI/Mw. La gelatina en solución que no contiene iones no coloidales distintos de H + y OH- se conoce como gelatina isoiónica. Densidad: 1543 kg/m³; 1,543 g/cm³: Masa molar: 13 212 g/mol: Punto de fusión: 508 K (235 °C) Propiedades químicas; Acidez: 2,16; 8,73 pK a: Familia: Aminoácido: Esencial: No: Codón: AAU, AAC: Punto isoeléctrico (pH) 5,41: Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo .Cuando el pH es igual al de su punto isoeléctrico (para la Alanina pH=6), está en su forma zwitterion, es decir, su amina está protonada y su ácido no (+H3N – CHR‘ – COO-), teniendo una carga positiva y otra negativa.El punto isoeléctrico, se calcula como la media de los valores de pKa de las etapas que forma y descompone el zwitterión. (d) Señale las diferencias entre proteínas globulares y fibrosas y ponga un ejemplo de cada una de ellas (0,5). En este artículo, profundizamos en los pasos esenciales, utilizando la palabra clave cómo calcular el punto isoeléctrico como nuestra guía. Se trata de un aminoácido no esencial, lo que significa que puede ser sintetizado por los humanos. Así, las propiedades moleculares de las caseínas facilitan procesos industriales para obtener productos con valor agregado, de ahí su importancia en la selección de leches con características deseables y de la optimización .
Alanina
La histidina es un precursor de la histamina, en la que se transforma mediante una descarboxilación. en nuestro ejemplo, el pi es 4. A este valor de pH la solubilidad de la sustancia es . La prolina ( Pro, P) o prolalina es uno de los aminoácidos que forman las proteínas de los seres vivos. (25 ℃ y 1 atm ), salvo que se indique lo contrario. También se eleva durante el embarazo y con los anticonceptivos.Punto isoeléctrico (pH) .- ¿Qué consecuencia tiene que el pH isoeléctrico de la histidina sea alrededor de 7,5? Ese valor es muy parecido al del pH fisiológico (pH ≈7), por lo que la histidina se puede comportar .Artículo revisado y aprobado por nuestro equipo editorial, siguiendo los criterios de redacción y edición de YuBrain. La carga neta de la molécula se ve afectada por el pH alrededor de su medioambiente y puede adquirir una carga más positiva o negativa debido a la ganancia o pérdida de electrones (H+). Es decir, puede tener grupos cargados (ionizados), pero la suma de todas las cargas positivas iguala a la de las negativas. Pregunta 20 5 pts.El punto isoeléctrico (pI) es el pH al que una molécula tiene carga eléctrica neta cero.Isoelectric point, the pH at which a particular molecule carries no net electrical charge, is an critical parameter for many analytical biochemistry and proteomics techniques, especially for 2D gel electrophoresis (2D-PAGE), capillary isoelectric focusing (cIEF), X-ray crystallography and liquid chromatography–mass spectrometry (LC-MS) IPC 2.Falso, ya que la solubilidad llega a su punto máximo en su punto isoeléctrico. El concepto es particularmente interesante en los aminoácidos y también en las .El punto isoeléctrico (pI) de la caseína es 4. Dibuja la estructura para el anión formado cuando la valina (a pH neutro) reacciona con una base. La solubilidad en agua de los péptidos es mínima en su punto isoeléctrico. El tipo B tiene un rango isoeléctrico más estrecho entre pH 4,7 y 5,4. Debido a su diversidad de propiedades, el caolín se utiliza en una amplia variedad de industrias y aplicaciones.
Carga de las biomoléculas
En el punto isoeléctrico la carga neta de la molécula es cero (0). En el hígado, la alanina se convierte en piruvato. La L-alanina se crea en las células musculares a partir del glutamato, en un proceso llamado transaminación.Usos Comunes del Caolín.Punto isoeléctrico.0: un grupo metilo, es la segunda cadena lateral más pequeña: valina : Val (V) Ácido 2-amino-3 . • Si el P H del medio es mayor que el punto isoeléctrico, entonces el medio es básico y el aa cede H +. En medio ácido, se encuentran protonados ambos grupos funcionales (catión), teniendo una carga positiva (+H3N – .El punto isoeléctrico de todas las caseínas está alrededor de 4,4 y 5,8, lo que favorece su precipitación bajo condiciones de acidez.
Punto isoeléctrico
Se trata del único aminoácido proteinogénico cuya α-amina es una amina secundaria (pirrolidina). Cada aa tiene su punto isoeléctrico característico. Si el pH fuera 6,5 el aminoácido tendría carga neutra ya que 6,5 es también el punto isoeléctrico del aminoácido.
Aminoácidos
Presenta un color ligeramente azulado. El pH de esta solución se conoce como punto isoiónico (pl). Estas soluciones . Los aminoácidos son moléculas orgánicas pequeñas con un grupo amino (NH2) y un grupo carboxilo (COOH). Dibujar la estructura para el catión formado cuando la valina (a pH neutro) reacciona con un ácido.Fórmula molecular: C 4 H 8 N 2 O 3 . Naturaleza hidrofóbica de Valina.Se llama pH isoeléctrico o punto isoelectrico al pH en el que la concentración de Zwitterión es máxima (el aminoácido no presenta carga neta). En el ARN mensajero está codificada como CCU, CCC, CCA, CCG. Nota: el servidor también se calcula el peso molecular (Mw) de los péptidos.La carga de una proteína va a depender del tipo de aminoácidos que la forman y del pH del medio en que se encuentre. (0,5) b) ¿Qué es el punto isoeléctrico de un aminoácido? (0,5) c) ¿Qué son los aminoácidos esenciales? (0,5) d) Señale las diferencias entre proteínas globulares y fibrosas y ponga un ejemplo de cada una de ellas. Los codones que codifican la cisteína son UGU y UGC (Uracilo GuaninaUracilo y UraciloGuaninaCitosina). lea el valor del punto isoeléctrico (pi) dado en la línea teórico pi / mw. Cada extracto obtenido se llevó a un pH de 4,0- 4,25 y 4,5 utilizando HCl 0,1 M, con el fin de abarcar el rango descrito en la bibliografía como puntos isoeléctricos de la proteína foliar [31].ingrese la secuencia de una letra del péptido: como ayuda en nuestro ejemplo, en el cuadro, y haga clic en calcular. Falso, ya que en laboratorio es necesario controlar el orden en que los aminoácidos se unen.• Se llama punto isoeléctrico al valor del pH en el cual un aminoácido adopta la forma dipolar neutra, esto es, presenta tantas cargas positivas como negativas. Además tampoco se desplazaría.
Estructura del aminoácido valina: explicaciones detalladas
La caseína representa cerca del 77% al 82% de las proteínas presentes en la leche y el 2,7% en composición de la leche líquida. La cantidad 1/κ 1 / κ es una medida para el tamaño de esta nube y κ κ es la longitud del debye-length. Lea el valor del punto isoeléctrico (pI) dado en la línea Teórica pI / Mw. Temas Selectos de Bioquímica General Elaborado por: Sergio F.08 Número CAS [63-68-3] PubChem: 876 Número EINECS: 200-562-9 Aminoácidos: La metionina (Met, M) es uno de los aminoácidos esenciales que forman las proteínas de los seres vivos. Todos los aminoácidos tiene la misma fórmula general: Isómero: .La teoría considera la vecindad de cada ion como una nube de cargas de signo opuesto similar a la atmósfera que cancela la carga del ion central (Figura 25. La gran cantidad de proteínas que se conocen están formadas únicamente por 20 aa diferentes.
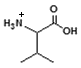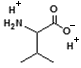
El pI es una propiedad constante de cada molécula.Respecto a las proteínas: (a) Dibuje la fórmula general de un aminoácido (0,5). Las constantes de ácido son las siguientes: pKa1 (carboxilo) a 2,34 y pKa2 (grupo amina) a 9,69. El pH isoelectrico se calcula como media de pK a,1 y pK a,2, es decir, la . En esta práctica se obtuvieron errores con los valores de pH registrados, por lo tanto los resultados no fueron los esperados. Ademas de consumirse en la leche, la caseína se utiliza en la elaboración pegamentos y pinturas, cubiertas protectoras, plásticos (como los usados en .El punto isoeléctrico (pI) es el valor de pH en el que una molécula tiene carga eléctrica neta cero.Cómo calcular el punto isoeléctrico.El punto isoeléctrico de una molécula puede tener implicaciones en diferentes procesos biológicos, como la interacción de proteínas con otras moléculas.Para Valina el punto isoeléctrico es 6. El concepto es particularmente interesante en los aminoácidos y también en las proteínas.La gelatina tipo A tiene un amplio rango isoeléctrico entre pH 7 y 9.El punto isoeléctrico (pI) o pH isoeléctrico (pH I) es aquel pH para el cual la molécula tiene carga neta cero. Utilizando la escala de ionización estime su PI con aproximación.En otras palabras para calcular el punto isoeléctrico de los aminoácidos, se debe seguir la siguiente fórmula, la cual justifica lo antes mencionado: pl = (pK1 + pK2) / 2.
Tarea Aminoácidos
Fórmula molecular: C 11 H 12 N 2 O 2; Masa molecular: 204,23 Punto isoeléctrico: pH=5. Referencias: Consejo de Educación Técnico Profesional. Se conocen otros 150 que no forman parte de las proteínas. Participa también en el desarrollo y manutención de los tejidos sanos, particularmente en la mielina que cubre las neuronas . En los aminoácidos los grupos ionizables corresponden a grupos carboxilos, amino, fenólicos y .
- Pyramiden Höhe – Verhältnisse in der Pyramide
- Punktioneneingriffe Anleitung : Operation: Vorbereitung, Ablauf und Reha
- Pula Beste Reisezeit – Beste Reisezeit Kroatien
- Python Float Eingabeparameter _ float() in Python
- Punch Arogunz Alter , Was ist mit Punch Arogunz‘ Augen los?
- Puschkin Museum | Puschkin-Museum (Moskau)
- Putzwerfer Obi _ Putzgitter kaufen bei OBI
- Psychologischer Fachberater _ Prüfungsordnung
- Punktförmige Hautblutungen : Purpura thrombozytopenische Bilder
- Psychovegetative Erschöpfung Beschwerden
- Python Dict Get First Key : Accessing Python dict values with the key start characters
- Pu Schaum Für Bauarbeiten _ Arten und Verwendung von PU-Dämmschaum