Natronlauge Leitfähigkeit Tabelle
Di: Samuel

Das Gesetz in 6 erlaubt uns also, die Gesamtleitfähigkeit als Summe der molaren Leitfähigkeiten aller in der Lösung befindlichen Ionen i zu berechnen: (7a) ideale Lösung: L F ( 0) = ∑ i Λ m, i 0 c i = ∑ i Λ e q, i 0 ∣ z i ∣ c i. Laugen färben Lackmus blau, Phenolphthalein . Je niedriger der µS/cm Wert, desto weniger Mineralien enthält das Wasser. Wenn du eine volle Natronlauge-Lösung hast, übertragen die positiv geladenen Ionen Elektronen an die negativ geladenen Ionen, was . Von Tobias Fendt • Zuletzt aktualisiert am 31. Mit jeweils neu zusammengestellten Lösungen wird der Versuch für die Temperaturen von 30°C und 35°C wiederholt. [mS]= 1 [Ω∙10 ] = [mA] [V] Die berechneten Werte sind in Tabelle 2 aufgeführt.Natronlauge leitet den elektrischen Strom, weil es eine Lösung aus Natrium- und Chloridionen ist.Temperaturkontrolle! Hydroxide sind Ionenverbindungen, die aus Metallionen und Hydroxidionen bestehen. Hohe Leitfähigkeitswerte können z. Natronlauge ist eine Lösung von Natriumhydroxid (NaOH) in Wasser. Natriumhydroxid (auch Ätznatron, kaustische(s) Soda), chemische Formel NaOH, ist ein weißer hygroskopischer Feststoff. Wenn wir in diesen Versuchsaufbau eine 0,5-molare Kochsalzlösung geben und 5 V Spannung anlegen, fließt 0,25 A. Ein Wasser mit pH = 2 ist also zehnmal saurer als bei pH = 3 oder hundertmal saurer als bei pH = 4 usw.Messaufbau zur Messung der elektrischen Leitfähigkeit einer Kochsalzlösung.3 Leitfähigkeit bei . ρ ˜ c-1 (Tabelle 1).Natronlauge – Reaktionsgleichungen.2 Leitfähigkeit bei starken Elektrolyten D00 – 4 1.Verschiedene Leitfähigkeiten in einer Tabelle. Foren-Übersicht. Unsere elektrische-Leitfähigkeit-Tabelle zeigt Ihnen die Mikrosiemenswerte von Wasser für unterschiedliche Reinheiten.
Leitfähigkeits-Titration von Cola
Chemikerboard
Gemäß Trinkwasserverordnung (TrinkV Anlage 3 zu § 7 und . Sie reagiert stark alkalisch und wirkt sehr stark ätzend auf viele Werkstoffe. So können wir uns den Alltag ohne Produkte wie Papier, Zellstoff, Seife oder Aluminiumfolie nicht vorstellen.

Diese Ionen sind elektrisch positiv und negativ geladen, was bedeutet, dass sie Elektrizität leiten können.Zur Messung der elektrischen Leitfähigkeit wird ein Mul-timeter als Amperemeter in Reihe und eines als Voltmeter parallel zum Stromkreis geschaltet. Flüssigkeiten, die bewegliche Ionen enthalten, leiten den elektrischen Strom.1 Bestimmung der Zellkonstanten der . Die Anfangswerte werden notiert.Mikrosiemens: Leitwert des Wassers erklärt.
elektrolytische Leitfähigkeit
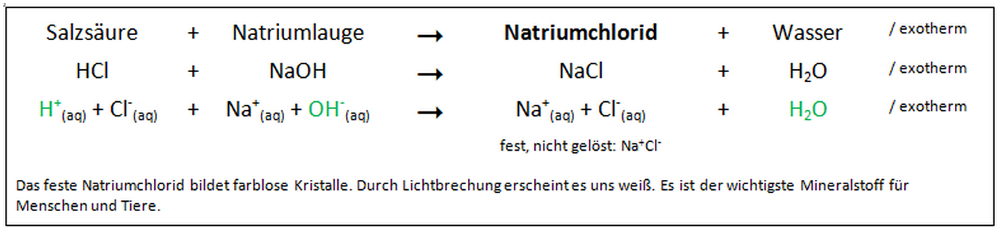
Prüft man die elektrische Leitfähigkeit von Natronlauge, so wird die Anwesenheit von Ionen bestätigt. Die Reaktion dieser Titration kann als Ionengleichung wie folgt formuliert werden: H + + Cl – + Na + + OH – → Na + + Cl – + H 2 O. Prüfe das Verhalten von Natronlauge gegenüber Lackmus- und Phenolphthaleinlösung. Betrachtet man aber Abbildung 14, ist deutlich zu erkennen, dass dies nicht der Fall ist.Destilliertes Wasser.
Natronlauge NaOH 50%
Leitfähigkeit besitzen (in (ohm-1*cm 2)/mol: H + 350, Cl- 76, Na + 51, OH – 192).Leitfähigkeit (22 °C) 80 – 100 mS/cm: Endotoxine: ≤ 2. In Elektrolytlösungen wird die Leitung des elektrischen Stromes von den hydratisierten Ionen übernommen. Die Leitfähigkeit von reiner Essigsäure bei Zugabe von Wasser wird über die Messung der Stromstärke verfolgt und in einer Tabelle sowie einem Diagramm aufgetragen. Die gelösten Salzmoleküle bilden in der Flüssigkeit Ionen, die für den Strom transLeitfähigkeit von Essigsäure beim Verdünnen. Anschließend werden 0,44 mL Essigsäureethylester zur Natronlauge hinzugegeben und alle dreißig Sekunden Spannung und Stromstärke notiert, bis die Werte sich über . Aus dieser Gleichung folgt, dass die Gesamtleitfähigkeit der Probenlösung im Verlauf der .

Ph Eur gewonnen.
Konduktometrie: Aufbau, Prinzip & Auswertung
Natriumhydroxid dissoziiert in Wasser zu Natriumionen (Na+) und Hydroxidionen (OH–). Salze liegen in wäßriger Lösung in Form hydratisierter Ionen vor, d. Elementverunreinigungen gemäß der Leitlinie ICH Q3D (Guideline for . Tragen Sie den Wert in die Tabelle ein.Widerstand bzw. Eine Lauge ist eine wässrige Lösung eines Hydroxids. Reines Wasser hat keine hohe Leitfähigkeit, aber je mehr Ionen hinzugefügt werden, desto höher ist die .Zur Messung der elektrischen Leitfähigkeit wird ein Multimeter als Amperemeter in Reihe und eines als Voltmeter parallel zum Stromkreis geschaltet.Konduktometrie: Titration Auswertung Berechnung Aufbau Leitfähigkeitstitration Anwendung Ablauf StudySmarter OriginalLeitfähigkeit L der Esterlösung abgelesen und notiert.Konduktometrie oder Leitfähigkeitsmessung ist eine chemisch-physikalische Analysemethode, die die elektrolytische Leitfähigkeit einer flüssigen Probe zur Bestimmung ihrer dissoziierten Inhaltsstoffe und deren Konzentration ausnutzt.2 µm Dieses Produkt wurde aus Natriumhydroxid Plätzchen Ph Eur, BP, JP, NF und water for injection USP hergestellt. Mithilfe des O hm’schen Gesetzes berechnen wir einen Widerstand R von 20 \ ( { {\varvec {\Omega}}}\) bzw.Die elektrische Leitfähigkeit liefert bei Gewässern erste Anhaltspunkte über den Zufluss von Niederschlagwasser und Abwasser. Vorausgesetzte Kenntnisse . Prüfmethode Rohstoffkenndaten Typischer Wert * Einheit . Um Aussagen etwas genauer zu machen, sind auch abgestufte Bezeichnungen wie schwach, sehr . bei vollständiger Dissoziation (α = 1) ist σ ˜ c bzw. (7b) reale Lösung: L F = ∑ i Λ m, i c i = ∑ i Λ e q, i ∣ z i ∣ c i. Leitfähigkeit, .
DOWNLOAD
der folgenden Tabelle angeführt: Leitfähigkeit bei 25 °C Reinstes Wasser 0,055 µS/cm Entionisiertes Wasser 1 µS/cm Regenwasser 50 µS/cm Trinkwasser 500 µS/cm Industrielles Abwasser 5 mS/cm Meerwasser 50 mS/cm 1 mol/L NaCl 85 mS/cm 1 mol/L HCl 332 mS/cm Auch reinstes Wasser besitzt eine Leitfähigkeit. Mit einer Weltproduktion von 60 Millionen Tonnen im Jahr 2010 gehört die Verbindung zu den bedeutendsten chemischen Grundstoffen und wird überwiegend in Form von . Daher hat man eine “neue Größe” definiert, die sogenannte Äquivalentleitfähigkeit. Von Anfang an kommt immer mehr Natronlauge dazu, deshalb steigt die Konzentration von Natrium-Ionen die ganze Zeit.
Die Fähigkeit von Stoffen, Energie (wie elektrischen Strom und Wärme) zu leiten, ist teilweise ähnlich ausgeprägt. Phosphorsäure ist eine starke Säure und liegt .Weitere Informationen Spezifische Leitfähigkeit von Flüssigkeiten Stoff chemische Formel beträchtlich an. ε = ε r ε 0
Natronlauge
1 Elektrische Leitfähigkeit – Grundlagen D00 – 1 1. Sie können entsprechend ihrer Ladungszahl z ein Einfaches oder Mehrfaches der . Das bedeutet, dass ein Hydroxid in Wasser gelöst wird, wobei Hydroxid-Ionen (OH –) freigesetzt werden.Ein Beispiel für eine Leitfähigkeitstitration ist die Säu r e-Base-Titration von Salzsäure mit Natronlauge.
Elektrische Leitfähigkeit im Wasser
Alkalische Lösungen, die auch als Laugen bezeichnet werden, sind wässerige Lösungen, in denen die Konzentration der Hydroxid-Ionen OH − die der Oxonium-Ionen H 3 O + übersteigt, was einen pH-Wert der Lösung von größer als 7 zur Folge hat. Säure-Base-Reaktion Cola enthält Phosphorsäure.
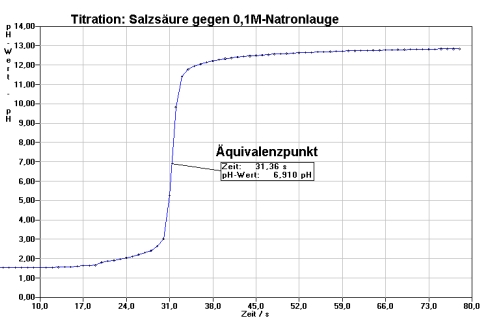
Titration
Die abgeleitete SI-Einheit der elektrischen Leitfähigkeit . die bereits im Kristall vorhandenen Ionen .Die Leitfähigkeit ist die Fähigkeit eines Materials – ob in Form von Flüssigkeit, eines Feststoffes oder von Gas -, elektrischen Strom zu leiten. Für die Zellkonstante K gilt folgende .Die Leitfähigkeit ist dabei der Kehrwert des spezifischen Widerstandes. Laugen sind Unterkategorien von Basen und haben somit alkalische Eigenschaften. Anschließend wer-den 0,44 mL Essigsäureethylester zur Natronlauge hinzugegeben und alle dreißig Sekunden Spannung und Stromstärke notiert, bis die . Gleichung (7b) ist . Sollte das der Fall sein, müsste man durch den Nullpunkt verlaufende Geraden erhalten. Dividiert man nun die Leitfähigkeiten bei den jeweiligen Konzentrationen durch die jeweilige Konzentration, so erhält man als Proportionalitätsfaktor die molare Leitfähigkeit (Dimension (früher): S ·cm 2 /mol), die je nach chemischer Natur des Salzes noch leicht von der Konzentration abhängt: ⇒ Λ m ( c) := ϰ c.Die elektrische Leitfähigkeit, auch als Konduktivität bezeichnet, ist eine physikalische Größe, die die Fähigkeit eines Stoffes angibt, elektrischen Strom zu leiten. Die Dissoziationsgleichung von Natronlauge lautet: NaOH + H2O → Na+ + OH– + H2O. Anhand dieser Werte werden dann die Abhängigkeiten der Leitfähigkeit erfasst. 0,5 bis 5 µS/cm. Tabelle 2: Leitwerte der verwendeten Metallsalzlösungen. Water for injection USP wurde für dieses Produkt aus purified water acc. Notiere hier die Messwerte: Stoff pH-Wert Natronlauge Calciumhydroxid-Lösung destilliertes Wasser 2. Tragen Sie den Wert in der Tabelle ein. auf Abschwemmungen von befestigten Betriebs- und Hofflächen nach Niederschlägen im Einzugsgebiet und Spitzenwerte im Winter auf den Einsatz von Streusalz im . Die Leitfähigkeit ist deshalb fast so hoch, wie . Bei vorgelegter Säure nimmt daher die Leitfähigkeit ab und zeigt auf Grund der stetigen Zugabe von Natronlauge im Überschuss wieder an.
Alkalische Lösung
Die elektrische Leitfähigkeit, auch als Konduktivität oder EC-Wert (vom englischen electrical conductivity) bezeichnet, ist eine Stoffeigenschaft und physikalische Größe, die angibt, wie gut elektrischer Strom geleitet wird.Leitfähigkeiten der gewöhnlichen Flüssigkeiten klein. Notiere deine Auswertung hier.Natronlauge, die wässrige Lösung von Natriumhydroxid, wird als sehr preiswerte und außerordentlich wichtige Grundchemikalie in fast allen Bereichen der chemischen Industrie vielseitig eingesetzt.Leitfähigkeit der Metalle dazu führen, dass es zu einer räumlichen Trennung der Reaktionen der Oxidation und Reduktion kommt.Elektrische Leitfähigkeit.Dabei gilt: Je verunreinigter ein Wasser ist, desto besser leitet es Strom.
Leitfähigkeitsmessungen
Molare Leitfähigkeit
Leitfähigkeit von Elektrolytlösungen. Konduktometer zur Bestimmung des Aschegehalts (entspricht dem Mineralgehalt) mittels . Löst man aber z.Leitfähigkeitsmessungen kennenzulernen, die Konzentrationsabhängigkeit der Leitfähigkeit im Fall starker sowie schwacher Elektrolyte experimentell zu erfassen und aus den ermittelten Leitfähigkeitswerten weitere charakteristische Größen der Elektrolytlösungen zu berechnen.Lauge – Definition. Eine bekanntes Beispiel ist Natronlauge (NaOH).4 DK-Kompendium Dielektrische Eigenschaften Die Dielektrizitätskonstante ε Die Dielektrizitätskonstante ε eines Isolators ergibt sich aus der Dielek-trizitätszahl ε r und der Dielektrizitäts- konstante ε 0 im Vakuum. Dies muss bei der Auswahl der richtigen Werkstoffe berücksichtigt werden.
Leitfähigkeitstitration
Die Oxidation führt zur Auflösung des Metalls, die Reduktion besteht in der Reaktion des Oxidationsmittels, in aller Regel Sauerstoff (neutrale und alkalische Medien) oder Hydronium-Ionen (saure Medien).3 Darstellung und Auswertung der Messergebnisse Zellkonstante K Die Leitfähigkeit der 0,01 M KCl- Lösung betrug 1,46 mS bei 20°C.Hier sollte eine Beschreibung angezeigt werden, diese Seite lässt dies jedoch nicht zu.
Äquivalentleitfähigkeit von Elektrolytlösungen
Bei verdünnten Lösungen, d.Die Steuerung eines bestimmten pH-Regimes ist vor allem bei schwankender Abwasserzusammenset-zung schwierig, da der pH-Wert bekanntlich eine logarithmische Größe darstellt. Als Leitfähigkeit wird die Fähigkeit eines leitfähigen chemischen Stoffes oder Stoffgemisches bezeichnet, [1] Energie oder andere Stoffe oder Teilchen im Raum zu leiten oder zu übertragen.Leitfähigkeit und Überführungszahl. Zu den Elektrolyten gehören die Lösungen von Säuren, Basen und Salzen sowie die Salzschmelzen.Deutung: Zum Vergleich der Leitfähigkeit der verschiedenen Metallsalzlösungen kann der Leitwert Germittelt werden. All dies sind Dinge, die es ohne Natronlauge nicht .
Leitfähigkeit
Messen Sie die Leitfähigkeiten und tragen Sie diese in die Tabelle ein. Diese hat ihre Ursa- .Natriumhydroxid und Natronlauge Name: Datum: Blatt 2 Aufgaben 1.Nach dem Äquivalenzpunkt steigt die Konzentration der Hydroxid-Ionen an. Welchen Unterschied stellst du zwischen den Lösungen und dem destillierten Wasser fest? Versuch 3: Untersuchung der elektrischen Leitfähigkeit
Hydroxide
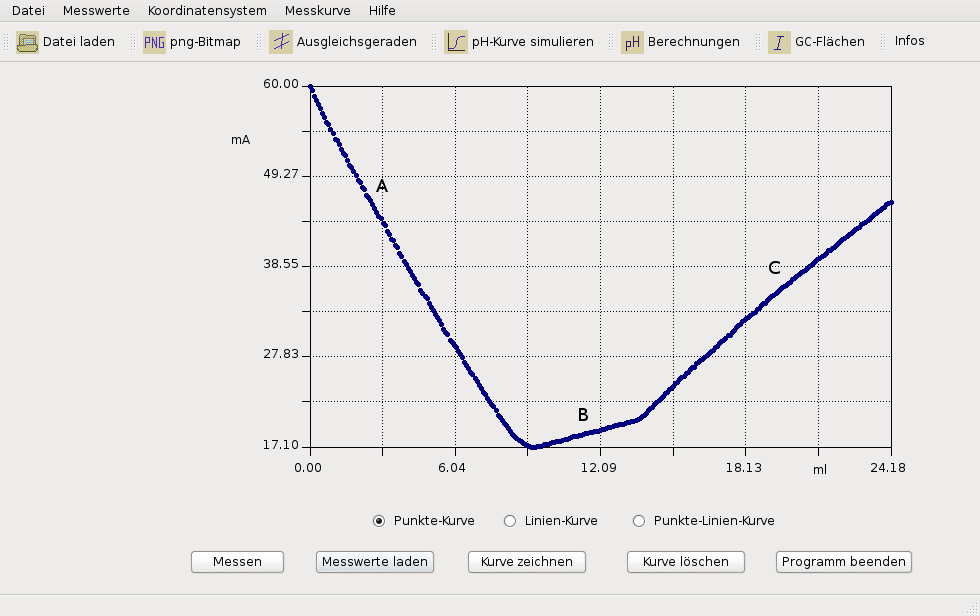
Am Ende sind viele Natrium-Ionen und Hydroxid-Ionen in der Lösung. Das gewählte Thema oder der Beitrag existiert nicht. Leitfähigkeit von Elektrolytlösungen müssen mit Wechselstrom gemessen werden, da bei Gleichstrom die Elektroden ›polarisieren‹, was die Feldverhältnisse ändert (Elektrodenvorgänge). Danach steigt die Leitfähigkeit der Lösung wieder bis auf \(\ce{1400\,\mu S/cm}\). Das Formelzeichen der elektrischen Leitfähigkeit ist ( griechisch sigma ), auch (gamma .Leitfähigkeit D 00 Konduktometrie Grundlagen Seite 1 / 20 AK-Computer – Materialien II – 04/97 Konduktometrie – Messung der elektrischen Leitfähigkeit Theoretische Grundlagen, Berechnungen und praktische Messungen Inhalt 1. Das Formelzeichen der elektrischen Leitfähigkeit ist σ (griechisch sigma) oder auch κ (griech. Die Äquivalentleitfähigkeit ist nichts anderes, als . Sie ist eine wichtige Messgrösse für viele Bereiche wie etwa im Trink- und Abwasserbereich, bei industriellen Herstellungsprozessen, bei der Qualitätskontrolle oder in der Lebensmittelbranche. Da die Leitfähigkeit sich proportional zur Konzentration der Ionen verhält, ist das Minimum der Kurve der Äquivalenzpunkt. Es ist also eine Base. in Wasser ein Salz, so steigt die elektrische Leitfähigkeit dieses Systems Tabelle 7./ml: Filtriert über 0. Nach obiger Gleichung für sollte die spezifische Leitfähigkeit proportional zur Elektrolyt-Konzentration sein. Die elektrische Leitfähigkeit wird in Mikrosiemens pro Zentimeter (μS/cm) gemessen. Die Leitfähigkeit nimmt zu.
Natronlauge 50% CAS 1310-73-2 zur Analyse EMSURE® – Find MSDS or SDS, a COA, data sheets and more information.Der Tiefpunkt der Leitfähigkeit ist bei einer Zugabe von fast \(\ce{4\,ml}\) Natronlauge erreicht. Die Leitfähigkeit liegt dann bei knapp \(\ce{800\,\mu S/cm}\). Bei der Leitfähigkeitsmessung eines starken Elektrolyten kann man sehen, dass die Leitfähigkeit stark konzentrationsabhängig ist. Geben Sie zur zweiten Glycinlösung 2 ml Essigsäure, und messen Sie die Leitfähigkeit. Geben Sie zur einen Glycinlösung 2 ml Natronlauge, und messen Sie die Leitfähigkeit.Leitfähigkeit. Die Leitfähigkeit wird durch das Vorhandensein von anorganischen gelösten Feststoffen (Ionen) und die Temperatur beeinflusst.
Natronlauge 0,5 mol/L CAS 1310-73-2
Natronlauge NaOH 50% Natriumhydroxid in wässriger Lösung Kurzbeschreibung Natronlauge ist eine klare, farblose, geruchlose und leicht viskose Flüssigkeit und mit Wasser in jedem Verhältnis mischbar.Natriumhydroxid in Form von Plätzchen.
einen Leitwert .
- Nanda Naveli Wikipedia : Fanaa: Ishq Mein Marjawan
- Narbengesicht Film : Sofia Helin
- Nasenmuschelhyperplasie Was Ist Das
- Natürliches Mittel Gegen Darmpilz
- Nautipox Farbkarte – Unterschiede, Einsatz und Besonderheiten
- Natürliche Locken Hervorbringen
- National Express Wembley _ The Eagles at Wembley Stadium
- Navigon Canada 310 Update : navigon canada 310 прошивка
- Nebenjob Chords – Nebenjob Chords
- Natürliche Locken Mit Glätteisen
- Nazareth Früher Und Heute | Impuls 213
- Natsume Yūjin Chō , Natsume Yūjin-chō