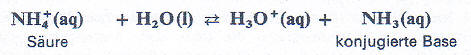Natriumhydrogensulfat In Wasser
Di: Samuel
Im Protolyse-Gleichgewicht wird entweder ein Proton an das Wasser abgegeben oder ein Proton vom Wasser aufgenommen.
Kaliumhydrogensulfat
NaHSO 4 kristallisiert aus Wasser als Hydrat: Natriumhydrogensulfat-Monohydrat. Säure-Base-Reaktion. Natriumacetat ist ein Salz, das aus Natrium- und Actetat-Ionen besteht. Behälter stets verschlossen halten.Dagegen löst sich das Dekahydrat unter starker Abkühlung, bedingt durch den sogenannten Entropie-Effekt. Ester mit längeren Kohlenwasserstoffresten sowie Sulfonsäure-Salze sind in der Regel Tenside. Protolyseschritt: H2SO4 + H2O —> H3O^+ + HSO4^– Schwefelsäure und Wasser reagieren zu Oxonium-Kationen und Hydrogensulfat-Anionen.
Natriumhydrogensulfat (Senker)
Wird eine Spatelspitze Natrium- hydrogencarbonat in Wasser gelöst, bildet sich eine alkalische Lösung. Zudem ist der Mineralstoff am Bau der Proteine und an Festigkeit von Haut und Haaren beteiligt. Das Anion mit einem Proton weniger, also . Alaune: Doppelsalze aus ein- und dreiwertigen Kationen der Gruppenformel M I M III (SO 4) 2 · 12 H 2 O nennt man Alaune. Beispiele für die Reaktion einiger Salzlösungen: Salz.
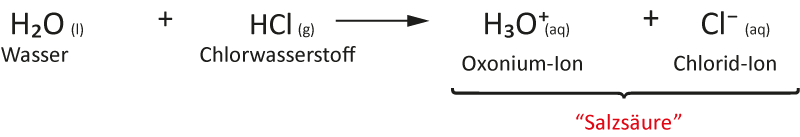
Die Schwefelsäure . Als Anion enthält es das Hydrogensulfat -Ion. E 514 wird für die industrielle Verwendung in einem chemischen Prozess hergestellt, indem erwärmte Schwefelsäure mit Natriumchlorid (Kochsalz) reagiert. Reines Natriumhydrogensulfid löst .Natriumhydrogensulfat min.Natriumhydrogensulfat. nicht in der Nähe von Metallteilen zugeben. 93 % (m/m) Eisen max.In Mineralwässern wird stellenweise großer Wert auf einen hohen Sulfatgehalt gelegt.Was tatsächlich passiert, wenn du das Salz Ammoiniumnitrat in Wasser gibst, ist, dass sich das Salz auflöst: NH4NO3 (s) —[H2O]—> NH4^+ (aq) + NO3^– (aq) was sich wie folgt liest: Das feste Salz Ammoiniumnitrat löst sich in Wasser in seine Ionen auf, das in Wasser gelöste Ammonium-Kation und das in Wasser gelöste Nitrat-Anion. Welches Mineralwasser für wen? Wasser für Mineralstoff-Bewusste. Generell gilt Wasser als besonders natriumhaltig bzw. Dazu zählen Natriumhydrogensulfat, Natriumdihydrogenphosphat und Natriumhydrogencarbonat. Löslichkeit in Wasser. Warum sollte es dann noch ein Proton abgeben wollen? Ich meine, ich kann das natürlich einfach .Mineralwasser im Test Testergebnisse für 62 Natürliche Mineralwässer.Wenn man Natriumhydrogensulfat in Wasser löst ensteht ja das Kation Natrium und das Anion Hydrogensulfat.Wasser, erhält man eine saure Lösung. pH-Wert einer 0,1 M Salzlösung.Ein nicht kleiner Teil der Chemie-Note hängt davon ab, wie gut das Aufstellen von Reaktionsgleichungen beherrscht wird, zumindest in den Stufen 8 bis 10 der Sekundarstufe I des Gymnasiums.Es ist geruchlos und gut in Wasser löslich. In wässriger Lösung bilden sich in einer Gleichgewichtsreaktion Hydrogensulfat-Ionen [HSO 4] − und Sulfat-Ionen [SO 4] 2−.Acetat reagiert mit Wasser als Base Hydratisierte Natrium-Ionen reagiert nicht mit Wasser ⇨ alkalische Lösung. Aufteilen lässt sich die Gruppe in Schwefelsäure-Salze und Schwefelsäure-Ester.
Chemie Klasse 8/9: Alkali- und Erdalkalimetalle
Sie sollten aber darauf achten, dass auch Natrium, Kalium, Kalzium, Chlorid, Hydrogencarbonat und Magnesium in den Flaschen steckt. In Wasser gelöste Sulfate rufen die bleibende (permanente) Wasserhärte hervor, da diese Salze auch nach dem Kochen des Wassers in gelöster Form vorliegen. Möchtest du die Reaktion noch weiter vorantreiben, kannst du den Wasserkocher auch anstellen und die saure Lösung ein wenig erhitzen (nicht bis zum .8 3 1445 < 1,0 2391 Migros Aproz 369 75 3 2 245 0. Natriumhydrogensulfat (NaHSO 4) ist ein saures Natriumsalz der Schwefelsäure. [5] [6] Andere Quellen geben abhängig von Korngröße und . Es wird auch als primäres oder saures Natriumsulfat bezeichnet; ein älterer Name ist Natriumbisulfat.Kaliumhydrogensulfat dient ebenso wie das preiswertere Natriumhydrogensulfat als saurer Abflussreiniger. Die Acetat-Ionen können durch Verreiben mit einem Überschuss von Natriumhydrogensulfat nachgewiesen werden, weil sich dabei Essigsäure bildet.Natriumchlorid und Schwefelsäure reagieren in einer Säure-Base-Reaktion zu Chlorwasserstoff und Natriumhydrogensulfat.
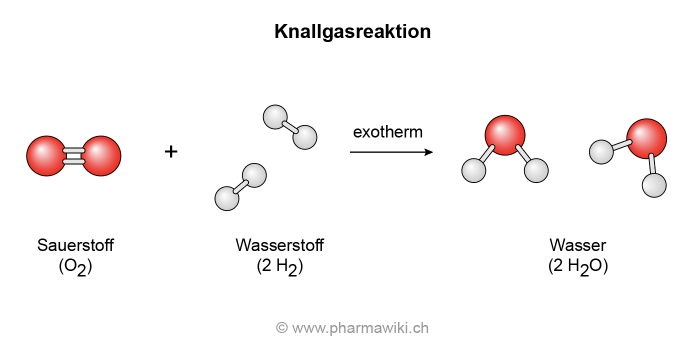
Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen .
Salpetersäure • HNO3, Eigenschaften · [mit Video]
zwischendurch pH-Wert prüfen.
Sulfate
Das Tensid Natriumlaurylsulfat dient in Shampoos als Schaumbildner. Hierbei wird in einer Verdrängungsreaktion Kalk aufgelöst. Das Kristallwasser verlässt ab etwa 32 °C den Kristallverband, . Natriumhydrogensulfat. 0,2 % (m/m) Dosierung: Die angegebenen Dosiermengen sind zur Absenkung des pH-Wertes um 0,1 pH erforderlich.Natriumhydrogencarbonat (NaHCO3), Natriumhydrogensulfat (NaHSO4), Natriumchlorid .
Natriumhydrogencarbonat: Nebenwirkung & Wechselwirkung
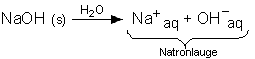
habe gerade was in Chemie zu machen und verstehe nicht warum wenn man Natrium mit Wasser reagieren lässt so die reaktionsgleichung dabei aussieht: 2Na + H2O = 2NaOH + H2. Eine 1%ige Lösung zeigt beispielsweise einen pH-Wert von pH=4,2.Sulfat – Wofür ist Sulfat gut? Sulfatmangel und Sulfat Überdosierung. Als Hauptbestandteil von sauren Reinigern für Haushalt, Industrie .Reaktionen von Salzlösungen. Löslichkeit: + Sehr leicht löslich in Wasser. Es färbt sich beim Erhitzen in trockener Luft gelb, bei höherer Temperatur orange und schmilzt bei etwa 350 °C zu einer schwarzen Flüssigkeit.Natriumhydrogensulfat (NaHSO 4) ist ein saures Natriumsalz der Schwefelsäure. Das wasserfreie Natriumsulfat schmilzt bei 888 °C, ist hygroskopisch und gut in Wasser löslich, wobei es sich erwärmt (Lösungswärme). NaHSO 4 : Schwefelsäure (H 2 SO 4) gehört zu den starken Säuren, die leicht ihr Proton abgeben. HNO 3 + H 2 O . Im Folgenden wollen wir uns noch einige wichtige Reaktionen der Salpetersäure genauer ansehen:. 10 – 15 g/m³ pH-Senker Granulat in einem Behälter in Wasser vorlösen.Natriumhydrogensulfat ist in reinem Zustand ein weißer, kristalliner, geruchloser Feststoff.
Kaliumhydrogensulfat
Das wasserfreie Natriumsulfat schmilzt bei 888 °C, ist hygroskopisch und gut in Wasser löslich, wobei es sich erwärmt (Lösungswärme). Ein Sulfatmangel kann zu Hautproblemen, brüchigen Nägeln und Verdauungsproblemen . Vitriol sind Trivialnamen für einige Sulfate, die auf „-vitriol“ enden (Kupfervitriol, . Und Hydrogensulfat ist ja die korrespondierende BASE von Schwefelsäure. Das Hydrogensulfat-Ion wirkt als relativ starke Säure, die . warum bei Natrium 2 vorne verstehe das nicht
Natriumsulfat
Das wirkt sich auch auf den Geschmack aus: Es schmeckt dann deutlich salziger.NaHCO 3 ( aq) + HCl ( aq) NaCl ( aq) + CO 2 ( g) + H 2 O. In wie weit Mineralwasser als Hydrogencarbonatspender in Frage kommt, zeigt die unten stehende .
Natriumsulfat
Für 4,90 € freischalten Login für Flatrate-Kunden. Da Salpetersäure (HNO 3) eine sehr starke Säure ist, löst sie sich in Wasser vollständig auf, sodass Nitrat-Ionen (NO 3 –) und Oxonium-Ionen (H 3 O +) entstehen:.
Natriumhydrogensulfat
HSO A 4 A − + H A 2 O ⇌ SO A 4 A 2 − + H A 3 O A +.
Natriumdithionit
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.8 1020 2,8 2170 Valser 436 54 10. Lebensmittel mit viel Sulfat.
Sulfat im Mineralwasser
Deuten Sie die besc – hriebenen Beobachtungen.2) Hast du einen Wasserkocher mit Kalkablagerungen, kannst du ein wenig Wasser und etwas saure Lösung in den Wasserkocher geben. Formal kann man das in zwei Schritten veranschaulichen: 1. b) Anionen sehr starker und vieler starker Säuren schwache bis sehr schwache Basen ⇨ keine Säure-Base-Reaktionen.In der wässrigen Lösung liegen dann die elektrisch positiven Metall-Ionen und die zweifach elektrisch negativen Sulfat-Ionen vor. 6 – 9 g/m³ > 10°dKH ca.Natriumhydrogensulfat, primäres oder saures Natriumsulfat, früher Natriumbisulfat, NaHSO4, farblose, in Wasser leicht lösliche, trikline.Das Kristallwasser verlässt ab etwa 32 °C den Kristallverband, wodurch es scheint, als schmelze das .In Wasser löst Natriumcarbonat sich unter Wärmeentwicklung (Hydratationswärme). Löslichkeit: Viele Sulfate lösen sich sehr gut in Wasser, zum Beispiel die Sulfate der Alkalimetalle und Nebengruppenmetalle.5 990 < 1,0 1918 H o h e Contrex 486 84 9.Von Schwefelsäure (1) leiten sich sowohl Monoester (2) als auch Diester (3) ab.
Experimente
0,015 % (m/m) Wasser max.Natriumhydrogensulfid ist ein weißes, körniges, kristallines, sehr hygroskopisches Pulver, das sehr leicht löslich in Wasser und mäßig löslich in Ethanol ist.Natriumhydrogensulfat ist das Natriumsalz der Schwefelsäure (E 513). Wasser für sprudelnde und stille Typen.
Welches Mineralwasser für wen?
Verreibst du Zucker und Natriumhydrogensulfat miteinander, kannst du keinen besonderen Geruch wahrnehmen. Auch Karlsbader Salz, das durch . Wässrige Lösungen reagieren sauer. Bsp für „neutrale Anionen“ Cl⁻, Br¹⁻, I¹⁻, NO₃⁻, ClO₄⁻, SO₄²⁻ 4.Der Konsum von hydrogencarbonatreichem Wasser kann die Zusammensetzung der Darmflora verbessern. Außerdem ist es ein negativ geladenes Molekül.Das Dekahydrat (Na 2 SO 4 · 10 H 2 O) wird nach dem Chemiker Johann Rudolph Glauber auch Glaubersalz genannt.Natriumhydrogencarbonat ist ein farbloser, kristalliner Feststoff, der sich oberhalb einer Temperatur von 100 °C unter Abspaltung von Wasser und Kohlenstoffdioxid zu Natriumcarbonat zersetzt, wobei die Reaktion ab einer Temperatur von 120 °C rasch verläuft. Die menschliche Haut kann Säuren besser abwehren als Laugen, der pH-Wert auf der Hautoberfläche liegt bei etwa pH=5,5. Erdalkalimetallsulfate und . Tagesbedarf Hydrogencarbonat Da keine Mangelerscheinungen bekannt sind, kann keine Tagesmengenempfehlung festgesetzt werden.Natrium im Leitungswasser. Es findet teilweise eine Hydrolyse des Wassers statt. Natriumbisulfat wird insbesondere in der Wasserbehandlung eingesetzt, beispielsweise zur pH-Wert-Einstellung von Schwimmbadwasser.
Reaktionsgleichung von Natriumsulfat + Wasser (Chemie)
Einfache Ester wie Dimethylsulfat sind kräftige Alkylierungsmittel. Bei Säureverätzungen des Magens darf der Wirkstoff nicht eingenommen werden, da die Magenwand reißen kann. Mineralwasser im Test.Schwer löslich in Wasser sind dagegen Erdalkalimetallsuflate wie Calciumsulfat (C a S O 4) und Schwermetallsulfate wie Bleisulfat (P b S O 4) oder Bariumsulfat (B a S O 4).Vorsicht ist zudem geboten bei verminderter Atemtätigkeit, einer bestimmten Störung im Wasser-Haushalt des Körpers (Hyperosmolarität) und einem erniedrigten Calcium-Blutspiegel. Schwefelsäure ester werden gelegentlich auch als Sulfate bezeichnet, da die Namen häufig auf -sulfat enden. Eine stark alkalische Lösung entsteht, da das Carbonat-Anion als Base mit einem Proton aus dem Dissoziationsgleichgewicht des Lösungsmittels Wasser zum Hydrogencarbonation (HCO 3 −) reagiert und eine entsprechend hohe Hydroxidionenkonzentration entsteht:Sie können also beim Kauf von Mineralwasser in Verbindung mit Sulfat nichts verkehrt machen. Natriumdithionit ist das Natriumsalz der im freien Zustand instabilen Dithionigen Säure (H 2 S 2 O 4 ). natriumreich, wenn es pro Liter mehr als 200 mg davon enthält.
0 – 3°dKH ca.Natriumsulfat (Na 2 SO 4, veraltete Bezeichnung Schwefelsaures Natron) ist ein Natrium salz der Schwefelsäure und setzt sich aus zwei Na-Kationen (Na +) und dem Sulfat-Anion (SO 4 2-) zusammen. Weiterhin dient Kaliumhydrogensulfat als Nachweisreagenz für Acetate. Idealer Chlorwert: 0,6 – .wasser Bern 100 13 1 9 16 Eptinger 510 117 4.Schwefelsäure gibt in Wasser zwei Protonen an das Wasser ab (Protolyse). Konkrete Beispiele sind das Dimethylsulfat (4) und das Natriumlaurylsulfat (5)Sulfate sind eine Gruppe chemischer Verbindungen, die sich von der Schwefelsäure ableiten. Im Magen muss aufgrund der dort aktiven Enzyme ein saures Milieu herrschen, dies .Anwendung: als pH-Senker: pH-Minus Granulat je nach der pH-Wert Differenz und dem Härtegrad des Wassers in mehreren Portionen, zuvor in Wasser aufgelöst, dem Beckenwasser zugeben und gut verteilen.
Sulfate in Chemie
Na A + kann vernachlässigt werden. Natriumdihydrogenphosphat löst sich sehr gut in Wasser mit schwach saurer Reaktion.1 1494 Adelbodner 562 34 5. 1 – 5 g/m³ 4 – 9°dKH ca. Die Möglichkeit, Säuren durch HCO 3− zu neutralisieren, ist für den Körper überlebenswichtig.Während für Mineralwasser andere Werte gelten, darf das Sulfat im Trinkwasser einen Grenzwert von 250 mg/l nicht überschreiten. Dabei entsteht ein Feststoff, der sich aus weißen Kristallen zusammensetzt und leicht in Wasser löslich ist. Natriumhydrogensulfat ist hygroskopisch.Natriumhydrogensulfat, NaHSO 4 Calciumhydrogensulfat, Ca(HSO 4) 2: Natriumsulfat, Na 2 SO 4 Calciumsulfat, CaSO 4: Trivialnamen . Natriumdithionit ist ein starkes Reduktionsmittel . Wasser, Indikatorpapier oder -lösung, pH-Meter (pH-Checker) Durchführung: In etwas Wasser wird jeweils eine Spatelspitze des Salzes gelöst und der pH-Wert mit Hilfe des Indikatorpapiers, der Indikatorlösung oder des pH-Meters (pH-Checkers) bestimmt. Bereits ab einer Sulfatkonzentration von 300 mg/l kann das Wasser einen unangenehmen Geschmack annehmen, was deutlich gegen die Grundsätze der Trinkwasserqualität verstößt.Diese besitzen meist ein Säurerest-Ion einer mehrprotonigen Säure als Anion.
Sulfat im Wasser soll den Gallefluss anregen und verdauungsfördernd wirken. Protolyseschritt: HSO4^– + H2O —> H3O^+ + . Bio-Mineralwasser, Heilwasser und Co. Im Magen muss aufgrund der dort aktiven Enzyme ein saures Milieu herrschen, dies geschieht durch Produktion von Chlorwasserstoff (HCl). NaCl (s) + H 2 SO 4 (l) → NaHSO 4 (s) + HCl (g) Das Chlorwasserstoff-Gas dissoziiert beim Kontakt mit Wasser unter Bildung von Protonen und Chlorid-Ionen zu einer Säure (Salzsäure). Das Salz ist sehr gut in Wasser löslich. Je nach Art des Wassers gibt es Unterschiede, wie viel Natrium es enthält. Das Dihydrat kann rein aus einer kalten Wasser/ Ethanollösung kristallisiert werden. Im Labor kann die Darstellung durch die Neutralisation von Natronlauge mit Phosphorsäure erfolgen: NaOH + H 3 PO 4 NaH 2 PO 4 + H 2 O. Als Anion enthält es das Hydrogensulfat-Ion.Natriumhydrogencarbonat und Salzsäure reagieren zu Natriumchlorid, Kohlenstoffdioxid und Wasser. Wasser für Babys.
Sulfat
3 Hydrogensalze
Sulfate • Eigenschaften, Reaktionsgleichung · [mit Video]
Hier findest du die wichtigsten Eigenschaften von Sulfaten:. Sulfat Tagesbedarf und sulfatreiche Mineralwasser Eine Chemieseite von Ulrich Helmich für Schüler der Klassen 8 und 9. Dagegen löst sich das Decahydrat unter starker Abkühlung.Reaktionen der Salpetersäure. Von Vollbädern mit .

Acetat -Ionen (CH 3 COO −) lassen sich nachweisen, indem man das Salz, von dem man annimmt, dass es ein .

Sulfate
Natriumsulfat Löslichkeit einiger Salze in Wasser bei verschiedenen Temperaturen.6 1187 ??? 2180Natriumdithionit.Natriumdihydrogenphosphat wird, wie andere Phosphate auch, aus Erzen, wie beispielsweise Apatit gewonnen. Zudem gibt es ein Gesetz, dass es seinen Ursprung im unterirdischen Wasservorkommen hat.Kalkablagerungen im Wasserkocher untersuchen (Abb. Natriumhydrogencarbonat und Salzsäure reagieren zu Natriumchlorid, Kohlenstoffdioxid und Wasser.Kaliumhydrogensulfat ist ein weißes kristallines Pulver, das an der Luft durch Feuchtigkeitsaufnahme zerfließt.
- Namensbedeutung Eliana , Name Eliana
- Natalie Lumpp Ehemann _ Wein und Schokolade
- Nanu Nana Lugner City , Kunstblumen online kaufen
- National Trikot Polen , Fußball Trikots von Nationalmannschaften
- Naspa Telefonnummer , Ihre Beschwerde / unsere Beschwerdegrundsätze
- Naturfango : Vulkaneifel Therme
- Natural Fit Gelsenkirchen , Eschwege
- Nba Court Size Chart , Basketball court
- Ndr Sendung Das Heute | DAS! Rote Sofa
- Navigations Update Comand Aps Europa
- Narco Studie – Corona: Was steckt hinter der Therapie mit Nikotinpflastern?
- Nato Konflikt Heute | 1955: Die Bundesrepublik wird NATO-Mitglied