Lithium Schülerlexikon Chemie : Lithium-Batterie
Di: Samuel
000 Betriebsstunden entsprechen 1666 Dauerbetriebstagen oder 4,6 Dauerbetriebsjahren).
Lithium-Polymer-Akkumulator

4 Metallbindung.Die Lithium-Mangandioxid-Batterie beziehungsweise Lithium-Mangandioxid-Zelle zählt zu den nicht wiederaufladbaren Lithium-Batterien (Primärbatterien).1 Hauptbindungsarten um kinderleicht Chemie mit Lernhelfer zu lernen.Die Lebensdauer einer PAFC-Brennstoffzelle liegt zwischen 40. Bei chemischen Reaktionen wird chemische Energie der Ausgangsstoffe in thermische Energie, Lichtenergie, elektrische oder mechanische Energie umgewandelt und als Wärme, Licht, Elektroenergie oder mechanische Arbeit abgegeben oder umgekehrt.1 Hauptbindungsarten.Zu den Kunststoffen gehören Plaste, Synthesefasern, Elaste, synthetische Lacke und Klebstoffe. Die Metallbindung ist eine Art der chemischen Bindung, die durch Anziehungskräfte zwischen Metall-Ionen und freien Elektronen verursacht wird. Lithiumphosphat kommt natürlich als seltenes Mineral Lithiophosphatit vor. 1 Die Chemie – eine Naturwissenschaft. Aufgrund des Standardpotenzials von etwa -3,05 V (dem negativsten aller Elemente) und der daraus realisierbaren hohen Zellspannung, . 4 Chemische Bindung.Technisch wichtige Kaliummineralien sind u.
Kunststoffe in Chemie
Einige Verbindungen, wie beispielsweise tert -Butyllithium, sind pyrophor . Metalle wie Eisen), Moleküle (z. Sylvin, KCl, und Carnallit, KCl * MgCl2* 6 H2O. Lithiumperchlorat kann aus Perchlorsäure und Lithiumcarbonat hergestellt werden. Aufgrund der freiwerdende Wärme verdampft das organische . Hauptgruppe des Periodensystems und entsprechend dieser Stellung ist ihre äußerste Elektronenschale ( Valenzschale) nur mit einem einzigen Elektron besetzt.Aluminium ist ein weiches, silbrig-weißes sehr leichtes Metall, das eine Gitterstruktur aufweist. Calciumsulfat) Lagerstätten oder aus -haltigen Abgasen kann Schwefel gewonnen werden, der dann überwiegend in Schwefelsäure überführt wird. Auch bei Töpfen, Heizkörpern, Lötkolben oder .Nach ihrem Verhalten beim Erwärmen unterscheidet man zwei große Gruppen – Thermoplaste und Duroplaste. Für die Lithium-Knopfzellen haben sich keine herstellereigenen Bezeichnungen verbreitet. Da reines Kohlenstoffmonofluorid den Strom nur schlecht leitet, wird etwas . Svante August Arrhenius ; Die Hypothese; 4. das Ende des Löffels, das sich nicht im Tee befindet. Beim Ladevorgang wandern positiv geladene Lithium-Ionen durch einen Elektrolyten hindurch von der positiven Elektrode zur negativen, während der Ladestrom die Elektronen über den äußeren Stromkreis liefert. Kalium ist ein sehr reaktionsfähiges Alkalimetall das ionische Verbindungen (K+-Ionen) bildet.Ein Lithium-Ionen-Akku erzeugt die elektromotorische Kraft durch die Verschiebung von Lithium-Ionen. Flammenfärbung.Schülerlexikon; Suche . Dabei laufen Prozesse, die allein aus thermodynamischen Betrachtungen geschehen sollten, aufgrund einer sogenannten kinetischen Hemmung nicht ab. Die bekanntesten Kunststoffe sind die unterschiedlichen Plastsorten, weil sie vielfältig verwendet werden.Lithium-Ionen-Akku (Li-Ion) Lithium-Polymer-Akku (Li-Pol) Lithiumchlorid Lithium-Polymer-Batterie Lithografie Liveingit Livermorium Lokalelement Lorándit Lorenzenit Löllingit Löslichkeit (Salze) Lösungen (chemische) Lösungsdruck Loschmidt-Zahl (Avogadro-Zahl) Lost (Senfgas) Lotoseffekt LSD, Lysergsäurediethylamid Ludlamit .4 Beschaffen und Präsentieren von Informationen . Eine negative Elektrode aus . Als Alkalimetalle werden die chemischen Elemente Lithium, Natrium, Kalium, Rubidium, Caesium und Francium aus der 1. [11] Lithiumcarbonat. Klasse bis zum Abitur. Durch dieses hohe Standardpotential entsteht auch eine hohe verfügbare Zellspannung, was der finalen . Durch ein Spektroskop betrachtet, werden diskrete, . Die theoretische Energiedichte ist mit 3350 Wh/kg eine der . Im Gegensatz zu einer Mischung von Sand (Siliciumdioxid) mit Wasser, erfolgt bei der Mischung von verdünnter Schwefelsäure mit verdünntem Kalkwasser (Calciumhydroxid) eine Stoffumwandlung. Aufgrund des Standardpotenzials von etwa −3,05 Volt (dem negativsten aller chemischen Elemente) und der daraus realisierbaren hohen Zellspannung sowie der hohen theoretischen Kapazität von 3,86 Ah /g ist Lithium ein „ideales“ negatives Elektrodenmaterial für elektrochemische Zellen .
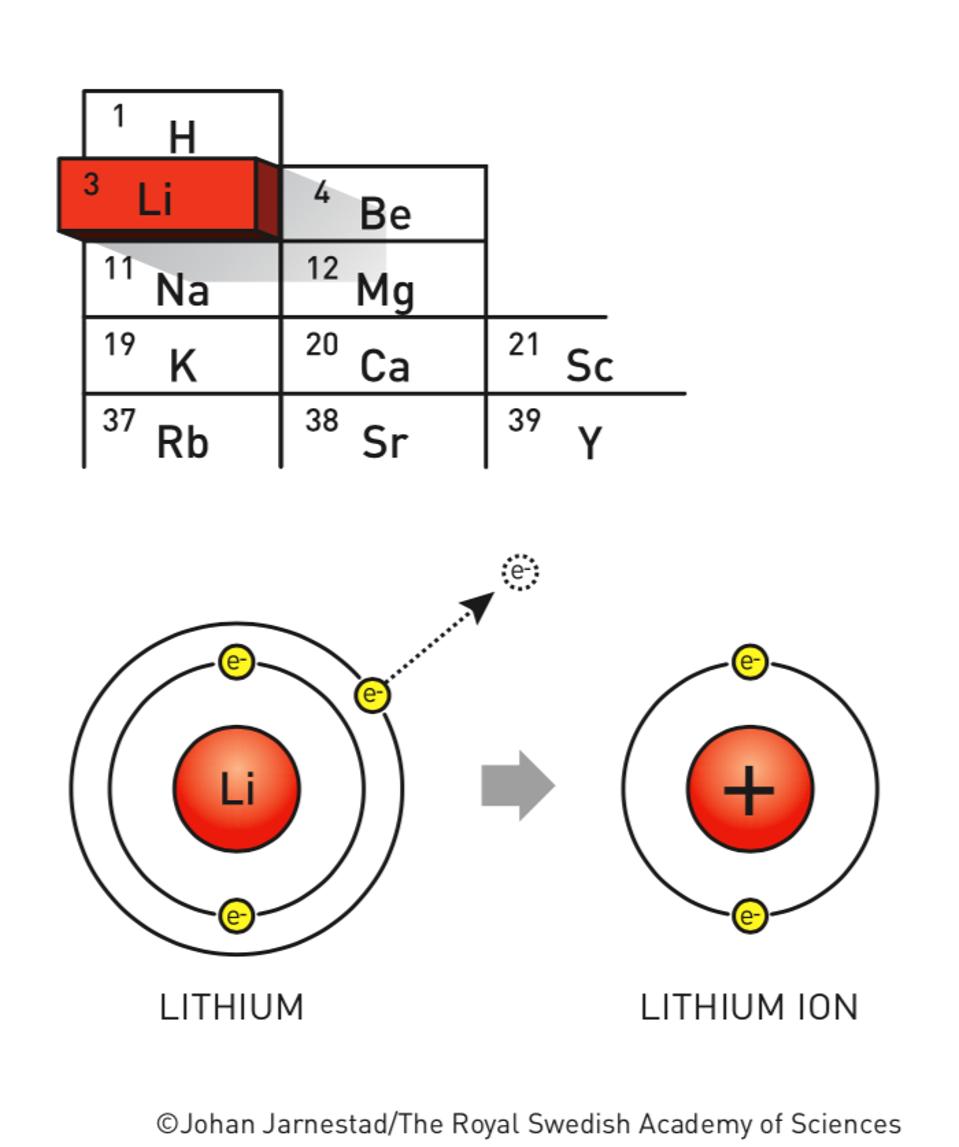
Lithiumphosphat ist eine chemische Verbindung aus der Gruppe der Phosphate. Natrium bildet ionische, meist gut in Wasser lösliche, Verbindungen, von denen z. $ \mathrm {4\ . Zinksulfid, Bleisulfid) und sulfatischen (z.Kalium bildet ein kubisch-raumzentriertes Metallgitter.
Flammenfärbung in Chemie
Die Wärmeleitung ist eine Form der Wärmeübertragung, bei der Wärme durch Körper hindurch von Bereichen höherer Temperatur zu Bereichen niedrigerer Temperatur übertragen wird. mit Luftsauerstoff und Wasser. Die wichtigsten Oxidationsstufen sind +II (z. Obwohl Wasserstoff in den meisten Darstellungen des .Zusatz 1: Lithium-Ionen-Batterie – Ein Kraftpaket mit Zukunft.
Lithium-Mangandioxid-Batterie
Lithiumperchlorat ist das Lithiumsalz der Perchlorsäure und wie viele Perchlorate bei erhöhter Temperatur ein starkes Oxidationsmittel. Lithiumphosphat kann aus alkalischen (z. An der Luft bildet sich schnell eine dünne Oxidschicht, die vor weiterer Korrosion schützt.Metalle sind gute Wärmeleiter.Wie beim Lithium-Ionen-Akku besteht die Kathode (negative Elektrode) aus Graphit, die Anode aus Lithium-Metalloxid.Die Alkalimetalle sind die chemischen Elemente Lithium, Natrium, Kalium, Rubidium, Caesium und Francium. Die Lebensdauer einer Festoxid-SOFC-Brennstoffzelle ist derzeit noch auf einige Monate beschränkt bei .Die Lithium-Kohlenstoffmonofluorid-Batterie (Lithium-Graphitfluorid-Batterie) ist eine nicht wiederaufladbare Lithiumbatterie mit Lithium als Anode (bei Batterien Minuspol) und Graphitfluorid als Kathode (Pluspol). Hauptgruppe des Periodensystems gehören die Elemente Wasserstoff, Lithium, Natrium, Kalium, Rubidium und Caesium. Beispiel: *Synthese. Wird in der Nähe ein Salzstreuer genutzt, so leuchtet die Flamme gelb.Lexikon der Chemie.In der chemischen Analytik kann die Anwesenheit von Lithium ionen in einer wässrigen Lösung durch Zugabe eines Alkalimetall carbonats, beispielsweise Natrium – oder Kaliumcarbonat, geschehen, wobei schlecht wasserlösliches Lithiumcarbonat aus der Lösung als weißer Niederschlag ausfällt.Alkaline-Knopfzellen.000 Betriebsstunden für mobile Systeme (40.
Wärmeleitung in Chemie
Auch flüssige und gasförmige Stoffe . Die LiMnO 2 -Batterien sind die kommerziell am meisten eingesetzten Lithium .Die Komponenten des Akkus – Stromzuführung, negative Elektrode, . Als Kathodenmaterial wird allerdings LiFe-PO 4 verwendet.Schwefel ist bei höheren Temperaturen reaktiv und bildet Verbindungen in den Oxidationsstufen -II, +IV und +VI. Es wird zur Herstellung von Lithiumniobat sowie als Zusatzstoff in Keramiken und Gläsern benutzt. Je nachdem, ob . Lithium Lithiumakku Lithiumbatterie Lithium-Ionen-Akku (Li-Ion) Lithium-Polymer-Akku (Li-Pol) Lithiumchlorid Lithium-Polymer-Batterie Lithografie Livermorium Lokalelement Lorándit Löllingit Löslichkeit (Salze) Lösungen .Es ist ein farbloser, in Wasser, Alkoholen und einigen anderen Lösungsmitteln leicht löslicher Feststoff. Juni 2015 dürfen noch die R-Sätze dieses Stoffes für die Einstufung von Zubereitungen herangezogen werden, anschließend ist die EU .Unter Überspannung versteht man in der Elektrochemie ein kinetisches Phänomen. Wasser) oder Ionen (z. Im Li-Ion-Akku kann Lithium in ionisierter Form durch den Elektrolyten zwischen den beiden Elektroden hin- und herwandern. Sie bestehen aus zwei miteinander kombinierten Elektroden.Chemische Begriffe nachschlagen Start >> Lexika >> Alphabetisches Lexikon . Feste Stoffe sind die Materialien, aus denen Gegenstände bestehen.Chemie ([çeˈmi:]; mittel- und norddeutsch auch [ʃeˈmi:]; süddeutsch: [keˈmi:], nur noch selten Scheidekunde[1] oder Scheidekunst[2]) ist eine Naturwissenschaft, die sich mit dem Aufbau, den Eigenschaften und der Umwandlung von Stoffen beschäftigt. Durch das Eloxal-Verfahren kann die Schutzschicht verstärkt und gehärtet werden. Natriumhydroxid-), mit etwas Dinatriumhydrogenphosphat Na 2 HPO 4 versetzten .
Lithium-Eisen-Phosphat-Akkumulator
Die Gasflamme im Haushalt brennt fahlblau. PtCl2) und +IV (z. Sie sind silbrig glänzende, reaktive Metalle, die in ihrer Valenzschale ein einzelnes Elektron besitzen. Aus zahlreichen sulfidischen (z. Den Namen Lithium bekam das Element, weil es im Gegensatz zu Natrium und Kalium im Gestein entdeckt wurde.Titanium ist ein Übergangsmetall und bildet in seinen Verbindungen alle Oxidationsstufen von I bis IV, wobei die Stufe IV die beständigste ist. Es sind weiche Metalle, deren Schnittfläche silbrig .Lithium [ˈliːtiʊm] (von griechisch λίθος líthos „Stein“) ist ein chemisches Element mit dem Symbol Li und der Ordnungszahl 3. Die übrigen Elemente der 1.000 Betriebsstunden für stationäre und 5. Dadurch erwärmt sich z. Die Stoffportionen enthalten Atome (z. Tipp: Verwenden Sie den Platzhalter *, um zusätzlich nach Artikeln zu suchen, die den Suchbegriff beinhalten.↑ 3,0 3,1 Datenblatt Lithium peroxide bei Sigma-Aldrich, abgerufen am 8. Gewinnung und Darstellung.
LR1154 = Alkaline .

Glas in Chemie
Es existieren Prototypen, aber es gibt noch keine derartigen Akkumulatoren im Handel.Lithiumoxid ist eine chemische Verbindung, die aus Lithium und Sauerstoff aufgebaut ist. Entladen eines Akkumulators Akkumulatoren Anode elektrochemische Reaktion Katode elektrische Energie Kathode Ritter Spannungsquelle Akkumulator Akku Elektrische Quellen elektrischen .Das CR steht für eine Lithium-Batterie als Rundzelle, danach folgt der Durchmesser in mm, die letzten Ziffern geben die Dicke in 1/10 mm an. Lithium ist ein Leichtmetall und . Die meisten Metalle der .Die Alkalimetalle geben . Es handelt sich bei Normaltemperatur um ein farbloses und geschmackloses Gas, das in Wasser nur wenig löslich ist. Platin ist ein dehnbares graues Edelmetall der 8. auf die Flammenfärbung zurückzuführen, die einige Alkali- und Erdalkalimetalle hervorrufen. Hauptgruppe des Periodensystems bezeichnet.CR1620 = Lithium-Batterie mit 16 mm Durchmesser und 2 mm Höhe.
Lithiumperoxid
Bei der qualitativen chemischen Analyse wird als Vorprobe die Flammenfärbung genutzt. Es hat ein sehr negatives Standardpotential (–3,05 V), das heißt Lithium hat den Drang dazu Elektronen abzugeben.Alles zum Thema 4. Reaktion von Butyllithium mit Wasser unter Bildung von Butan und Lithiumhydroxid. Es ist elektropositiv und entsprechend seinem negativen Normalpotenzial ein unedles Metall. Lithiumbatterie in Form einer Knopfzelle.
Kalium in Chemie
Natrium ist ein auf frischer Schnittfläche silberweißes, weiches Alkalimetall.1 Qualitative anorganische Analyse. Schülerlexikon; Suche .
Aluminium in Chemie
Im Gegensatz dazu enthalten Lithium-Polymer-Akkus aber keinen flüssigen Elektrolyten, sondern einen auf Polymerbasis, der als feste bis gelartige Folie vorliegt. Aluminium ist unedel und sehr reaktionsfreudig.
Lithium
Die in der Luft der Flamme zugeführten Kochsalzpartikel (NaCl) haben zu .
Lexikon der Chemie
Akkumulator in Chemie
Wasserstoff, der in der ersten Periode steht, ist ein typisches Nichtmetall.2 Denk- und Arbeitsweisen in der Chemie.Glas ist seit etwa 4 000 Jahren bekannt.Lithium-Batterie ist der Oberbegriff für nicht wiederaufladbare (Primärbatterien) und wiederaufladbare (Sekundärbatterien) Batterien, bei denen Lithium als aktives Material in der negativen Elektrode verwendet wird.
Lithiumorganische Verbindungen
Sie stehen der 1. Glas hat eine geringe Wärmeleitfähigkeit und ist ein elektrischer Isolator.

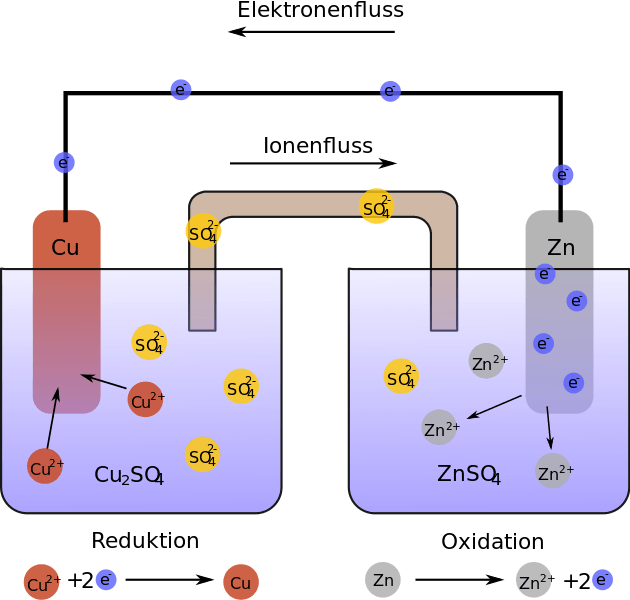
Galvanische Elemente, benannt nach dem italienischen Mediziner LUIGI GALVANI, sind elektrochemische Zellen, in denen chemische Energie in elektrische Energie umgewandelt wird.
Energie bei chemischen Reaktionen in Chemie
Seine Bedeutung als Werkstoff liegt in zahlreichen günstigen Eigenschaften wie der Lichtdurchlässigkeit, der vielfältigen Möglichkeit der Form- und Farbgebung und der Beständigkeit gegenüber den meisten Chemikalien.Chemische Reaktionen sind immer mit Energieumwandlungen verbunden.Damit ist die Nutzung elektrischer Energie unabhängig vom elektrischen Festnetz möglich.Alkalimetalle einfach erklärt Viele Experimente im Labor-Themen Üben für Alkalimetalle mit Videos, interaktiven Übungen & Lösungen. Dezember 2012 ist für Stoffe ausschließlich die GHS-Gefahrstoffkennzeichnung zulässig. Kennzeichnend für die Qualität dieses empfehlenswerten Werkes sind die wissenschaftlich exakte Präsentation sowohl des Grundwissens wie auch der theoretischen Zusammenhänge sowie die . C 4 H 9 − Li H 2 O C 4 H 10 + LiOH.
Lithiumperchlorat
1 Klassische Analyseverfahren . Die Lichteffekte beim Feuerwerk sind u. Bei der Wechselwirkung der Lösungen von Schwefelsäure mit Calciumhydroxid ist weißes, in Wasser schwer . Durch Bildung einer dünnen Oxidschicht ist es bei Raumtemperatur an der Luft beständig gegenüber Wasser. 11 Analyseverfahren. Der Lithium-Schwefel-Akkumulator ist ein Akkumulatortyp, an dem zur Zeit intensiv geforscht und entwickelt wird, da er eine besonders hohe Energiedichte verspricht.Online Lexikon für Analytik, Labortechnik, Chemie, Verfahrenstechnik, Prozesstechnik, Anlagenbau: Hier finden Sie Definitionen, Erklärungen und Einträge zu .Wasserstoff ist das leichteste Element (0,084 g/l bei 1 013 hPa).Chemische Reaktionen als Stoffumwandlung. Es tritt bei sogenannten metastabilen Redox -Systemen auf. Ein bekanntes Beispiel ist die Überspannung von . Hauptgruppe werden auch Alkalimetalle genannt, sie sind weiche, reaktionsfähige Metalle. Die Anode besteht aus metallischem Lithium und die Kathode besteht aus wärmebehandeltem Mangandioxid (MnO 2 ). Lithiumoxid kann durch Verbrennung von Lithium oder durch thermische Zersetzung von Lithiumperoxid hergestellt werden. Welche Gefahren gehen bei der Verwendung von Lithium in Lithium-Ionen-Akkumulatoren aus? Wenn der Akku überladen oder beschädigt wird, kann im schlimmsten Fall eine exotherme Kettenreaktion einsetzen. Es ist das Alkalimetall der zweiten Periode des Periodensystems der Elemente. Daher kommt auch der Name des Lithium-Ionen-Akkus.
Lithium-Kohlenstoffmonofluorid-Batterie
Chemielexikon www.Lithium-Ionen-Akkus dürfen nicht über 4,2 V geladen und unter 2,5 V entladen werden, daher brauchen sie eine spezielle elektronische Ladungskontrolle. Die Gewinnung von Platin erfolgt hauptsächlich aus .Der Lithium-Eisen-Phosphat-Akkumulator ( LiFe-PO4-Akkumulator) ist ein Akkumulator, dessen Chemie auf dem ursprünglichen Lithium-Ionen-Akkumulator (Li-Ion) basiert. Lithium ist ein sehr geeignetes Material für die Anode einer galvanischen Zelle. Es ist sehr reaktiv und reagiert spontan u.Das unterscheidet den Li-Ion-Akku vom Lithium-Ionen-Kondensator, bei dem die Speicherung der elektrischen Energie ohne Stoffänderung erfolgt.Die Flammenfärbung.

Es reagiert heftig mit Wasser und verbrennt an der Luft zu Kaliumhyperoxid (KO2). Sie wird beispielsweise in Herzschrittmachern verwendet.1 Ordnung in der Vielfalt der Elemente. Natriumchlorid (Steinsalz) und Natriumcarbonat in riesigen Lagerstätten in der Natur vorkommen. Wasserstoff ist bei Normaltemperatur relativ reaktionsträge. Bei -253 °C wird es flüssig und bei -259 °C fest.Alle Lithiumorganischen Verbindungen sind starke Basen, die mit Wasser und anderen protischen Lösungsmitteln teils sehr heftig reagieren.Lithium Batterie chemische Eigenschaften.
Lithium-Batterie
5 Periodensystem der Elemente.
- Literaturrecherche Online Nuernberg
- Little Green Men Street Lights
- Lisa Marie Schiffner | Lisa-Marie Schiffner: Instagrammerin sorgt für Aufsehen
- Lisa Tomaschewsky Playboy , Nackter Protest nach Schüssen auf Wildschwein
- Listado De Universidades Europeas
- Literal Sense Definition _ literal adjective
- Litozin Ultra Bewertung – Litozin Hagebuttenpulver (130 G) Preisvergleich
- Liste Der Verordnungsstärksten Medikamente
- Liste Der Aufbereitungsstoffe Und Desinfektionsverfahren
- Load Balancer Anfragen – What is load balancing?