Lioh Löslichkeit – Lithium (Li)
Di: Samuel
Bei dem Lösen des Alkalioxids in Wasser entsteht ein Alkalihydroxid. Die Löslichkeit eines Stoffes gibt an, in welchem Umfang ein Reinstoff in einem Lösungsmittel gelöst werden kann. Universität Universität Koblenz-Landau.Lithiumhydrid LiH ist eine salzartige chemische Verbindung von Lithium und Wasserstoff. 62, Stellung 2). Chemie (73030010) 38 Dokumente. Glasstab zur Kristall- NS in wenig HCl lösen und (NH 4) 2 SO 4 Lsg. Weiterhin bildet es keine Hydrate, wie sie von den anderen Lithiumhalogeniden bekannt sind.a HgS PbS Bi 2 S 3 CuS CdS II.
Lithiumphosphat
Die Löslichkeit in Wasser beträgt nur 1,3 g/l. Hochgeladen von: Anonymer Student. · Dichte und/oder relative Dichte · Dichte: Nicht bestimmt.
Trennungsgang der Kationen
Löslichkeit bezeichnet die Eigenschaft des Stoffes, sich unter homogener Verteilung (als Atome, Moleküle oder Ionen) im Lösungsmittel zu vermischen, d. Die Herstellung erfolgt daher durch Umsetzung von wässrigen Lithiumsalzlösungen mit .Lithiumhydroxid (LiOH) Natriumhydroxid (NaOH) Kaliumhydroxid (KOH) Rubidiumhydroxid (RbOH) Cäsiumhydroxid (CsOH) Calciumhydroxid (Ca(OH) 2) Strontiumhydroxid (Sr(OH) 2) Bariumhydroxid (Ba(OH) 2) Es sollte beachtet werden, dass die drei Erdalkalimetallhydroxide (Kalzium, Strontium und Barium) in Wasser schlecht . Neben dem Löslichkeitsprodukt existiert auch noch eine etwas griffigere Definition der Löslichkeit eines Feststoffes: die molare Löslichkeit. Für die zivile Energiegewinnung wäre die kontrollierte Kernfusion von 6Li und 2D geradezu ideal: es entsteht nur Helium und sehr viel Energie. Es werden hier lediglich Alltagschemikalien eingesetzt, die den Schülerinnen und Schülern aus ihrer Alltagswelt bekannt sind. Lithium geht eine große Zahl von Reaktionen mit organischen Reaktionsmitteln sowie mit anorganischen Reaktionsmitteln ein. Ammon Ist die organische Alkoholschicht blau gefärbt, so sind Cobalt-Ionen anwesend.Lithiumcarbonat (Li 2 CO 3), das Lithiumsalz der Kohlensäure, bildet farblose Kristalle mit einem Schmelzpunkt von 720 °C und einer Dichte von 2,11 g·cm-3.Ihr Wert steigt mit der Flüchtigkeit, sinkt also mit steigender Löslichkeit. [3] [7] Beim Erhitzen im Vakuum gibt sie oberhalb von 300 °C Ammoniak ab.Löslichkeit: reagiert mit Wasser.
Löslichkeitsprodukt • Formel und Berechnen · [mit Video]
Das ist keine chemische Reaktion sondern ein Lösevorgang / Dissoziation oder Hydratation (Solvation in Wasser).
Der qualitative Trennungsgang
Praktikum Anorganische Chemie/ Kationentrennungsgang
Löslichkeit
Als Zwischenstufen entstehen Lithiumamid . Bei Raumtemperatur ist es ein farbloses, hygroskopisches kristallines Pulver, das leicht bittermandelartig riecht. Akademisches Jahr: 2018/2019. [1] Die Trennung zwischen Lösungsenthalpie und Reaktionswärme .H260: In Berührung mit Wasser entstehen entzündbare Gase, die sich spontan entzünden können.
Alkalimetalle und Wasser
zutropfen: isation gebracht werden.

Wovon ist die löslichkeit abhängig?
Die Verbindung ist in Wasser, Alkohol, Ether, Pyridin und Nitrobenzol sehr löslich (Royal Society of Chemistry, 2015). mit LiOH/KNO 3 – Lösung lösliche Thiometallat- bzw. Es ist das das einzige . Die Sulfide von Hg, Pb, Bi, Cu und Cd (Kupfer-Gruppe) lösen sich nicht und bleiben zurück. durch katalytische Oxidation mit Distickstofftetroxid in Anwesenheit von Sauerstoff hergestellt. · Partikeleigenschaften Nicht bestimmt · Sonstige Angaben · Aussehen: · Form: Pulver · . Es gibt aber auch feste Lösungen, wie etwa bei Legierungen, Gläsern, keramischen Werkstoffen und dotierten Halbleitern.Die hohe Aktivitätssteigerung durch die LiOH-Beschichtung lässt sich nicht mit der höheren Löslichkeit des Ammoniaks in LiOH erklären. SrSO 4 Filtrat der SrSO 4 Fällung weiß ammoniakalisch stellen, er- wärmen und (NH 4) 2 C 2 O 4 zugeben: CaC 2 O 4 weiß Dipl. [6] 2 LiH → 900 − 1000 o C 2 Li + H 2 ↑. Dieses Dokument wurde von einer bzw. Der Wasserstoff kann durch Reaktion mit . [2] Die Verbindung ist allgemein sehr hydrolyseempfindlich und greift Glas schwach an.
Online-Rechner: Rechner für pH einer Lösung
Da Lithiumhydrid sehr stabil ist, stellt es in Verbindung mit der niedrigen molaren Masse des Lithiums einen hervorragenden Wasserstoffspeicher mit einer Kapazität von 2,8 m³ Wasserstoff pro Kilogramm dar. Zumeist ist das Lösungsmittel eine Flüssigkeit. Das kannst du gut anhand der Henderson Hasselbalch Gleichung .Alternativ kann man die zuvor beim Lösen von Nickelsulfid und Cobaltsulfid erhaltene Lösung nochmals mit konz. Aus konzentrierten wässrigen Lösungen kristallisiert wasserfreies Lithiumchlorid erst bei Temperaturen oberhalb von 98 °C aus. [3] Es kommt auch als Lithiumphosphat-Hemihydrat Li 3 PO 4 ·½H 2 O vor. P231+P232: Inhalt unter inertem Gas handhaben und aufbewahren. Stoffmengenkonzentration ( c l {\displaystyle c_{\mathrm {l} }} mit Index l für engl. LiPF 6 ist das Lithiumsalz der unbeständigen Hexafluorophosphorsäure.Die Sulfide von As, Sb und Sn ( Arsen-Gruppe) bilden also mit dieser Ammoniumpolysulfidlösung (NH 4) 2 S x – bzw.Metallisches Lithium ist in kurzen allphatischen Polyaminen sowie in Etyhlamin löslich.Löslichkeit: exotherme Reaktion mit Wasser. In flüssigen Lösungsmitteln nimmt die Löslichkeit von Gasen mit steigender Temperatur ab. Wässrige Lösungen reagieren leicht alkalisch (pH 8).Es gibt auch nicht viele starke Basen, und einige von denen sind nicht sehr löslich im Wasser. Lithiumoxid ist eine chemische . Es reagiert mit Sauerstoff zum Formmonoxid und -hyperoxid. · Relative Dichte Nicht bestimmt.Natriumcyanid ist das Natrium salz der Blausäure (HCN). Sie reduzieren den Wasserdampfdruck um ca. Je höher die Temperatur des Mineralwassers ist, desto weniger Kohlenstoffdioxid ist darin lösbar.The table below provides information on the variation of solubility of different substances (mostly inorganic compounds) in water with temperature, at one atmosphere pressure.Lithiumhydroxid-Monohydrat ist eine anorganische Verbindung mit der chemischen Formel LiOH x H 2 O.
Was sind starke Basen?
Löslichkeit von Salzen
Ein solcher Ablauf ist bislang jedoch nur kurzzeitig und bei Plasmatemperaturen möglich (>106 °C).
Henry-Gesetz
Lithiumhexafluorophosphat ist eine anorganische Verbindung bestehend aus Lithium, genauer dem Kation Li +, und dem Hexafluorophosphat -Anion PF 6−, so dass die Summenformel LiPF 6 resultiert. Es läst sich nicht in Kohlenwasserstoffen lösen. Beim Erhitzen im Stickstoff strom bildet sich Lithiumnitrid. Lithiumhydrid beginnt bei 900-1000 °C, sich in elementares Lithium und Wasserstoff zu zersetzen und ist damit das bei weitem hitzebeständigste Alkalihydrid. Bezogen auf den eingesetzten Träger adsorbiert auf dem unmodifiziertem Puralox dieselbe Menge .Lithium – Eigenschaften.CH 2 O + LiH + H 2 O CH 3 OH + LiOH. Die Löslichkeit eines Stoffes gibt an, ob und in welchem Umfang ein Reinstoff in einem Lösungsmittel gelöst werden kann. Schwerlösliches Salz: Liegt die Konzentration eines gelösten Stoffes unter . Der Siedepunkt von Lithium beträgt. · Dampfdichte Nicht anwendbar.Gesamtniederschlag mit LiOH / KNO 3 Lsg. Im Labor kann der Thioether Dimethylsulfid mit stöchiometrischen Mengen Wasserstoffperoxid oder verdünnter Salpetersäure oxidiert werden. Beispiel: Lithiumoxid und Wasser reagieren zu Lithiumhydroxid. Der quantitative Abbau zu Lithiumimid erfolgt jedoch erst bei 400 °C und erst oberhalb 750–800 °C .

P223: Keinen Kontakt mit Wasser zulassen. Hierdurch kann (fachlich korrekt) das Salz in leichtlöslich oder schwerlöslich eingeteilt werden.

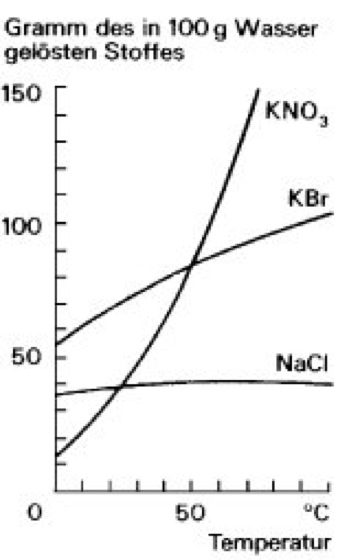
Lithiumchloridlösungen sind stark hygroskopisch. · Dampfdruck: Nicht anwendbar.Löslichkeit bei verschiedenen Temperaturen Innerhalb dieses Versuches soll die Löslichkeit in Abhängigkeit von der Temperatur beobachtet werden. Die einzelnen LiOH Bauteile werden aus dem Kristallverband gelöst indem die Ionen eine Hydrathülle erhalten. H- und P-Sätze: H: 272 ‐ 314: P: 220 ‐ 280 ‐ 305+351+338 ‐ 310: Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.Lithiumamid ist ein farb- und geruchloser Feststoff, der sich in Wasser zersetzt. Die Löslichkeit von Gasen steigt mit zunehmendem Druck.Darstellung und Gewinnung. Die Löslichkeit in Wasser beträgt ca. Studierenden haben 38 Dokumente in diesem Kurs geteilt. GESTIS ist das Gefahrstoffinformationssystem der Deutschen Gesetzlichen Unfallversicherung. liquid), Molalität ( b {\displaystyle b} ) und Stoffmengenanteil ( x . einem Studierenden hochgeladen, die/der wie du beschlossen hat, anonym zu bleiben. Das farblose, kristalline Pulver wird hauptsächlich in . Lithiumoxid reagiert leicht mit Wasserdampf unter Bildung von Hydroxid und mit Kohlendioxid unter Bildung von Carbonat; Daher muss es in einer sauberen und trockenen Atmosphäre gelagert und gehandhabt werden. Er kristallisiert orthorhombisch mit den Gitterkonstanten a=6,12 Å, b=10,53 Å und c=4,93 Å mit der Raumgruppe Pmnb (Raumgruppen-Nr.Molare Löslichkeit. Die Ammoniumcarbonat-Gruppe . Wenn eine Säure (HA) und ihre korrespondierende Base (A –) in wässriger Lösung in den gleichen Konzentrationen vorkommen, dann sind auch pH-Wert und pKs Wert identisch. Im Gegensatz dazu gilt: Je höher der Druck ist, desto mehr Kohlenstoffdioxid ist im . Die folgenden sind wasserlöslich – Natriumhydroxid NaOH – Kaliumhydroxid KOH – Lithiumhydroxid LiOH – Rubidiumhydroxid RbOH – Cäsiumhydroxid CsOH. Es ist ein weißes kristallines Material, das mäßig löslich in Wasser und schwach löslich in Ethanol ist. \pu {181°C} 181 ∘C. Technisch wird Dimethylsulfoxid aus Dimethylsulfid z.· Löslichkeit · Wasser: Nicht bestimmt.L Löslichkeit, Drall, Drehimpuls, Induktivität, Leucht- / Strahldichte Einheit: Liter M Molare Masse (in g/mol), (Licht-)Ausstrahlung, Magnetisierung Vorsilbe: Mega N Teilchenzahl (in Stück), N A = Avogadro -Konstante H314: Verursacht schwere Verätzungen der Haut und schwere Augenschäden. Das Lithiumhydroxid-Monohydrat von AMG ist eine Qualität für .Die Sulfide von As, Sb und Sn (Arsen-Gruppe) bilden also mit dieser Ammoniumpolysulfidlösung (NH 4) 2 S x – bzw. Im Folgenden lernst du die physikalischen Eigenschaften von Lithium kennen: Lithium ist ein silberweißes und weiches Metall. Units of solubility are given in grams per 100 millilitres of water (g/100 mL), unless shown otherwise. 450 g LiCl/kg Lösung. Bei niedrigeren Temperaturen erhält man eine der Hydratformen. Anhand dem Löslichkeitsprodukt (siehe entsprechendes Kapitel bei Lernort-Mint) kann die Löslichkeit eines Salzes (in der Regel in Wasser) bestimmt werden. Es gibt mehrere Varianten der beiden fundamentalen Typen, da es viele Wege gibt, die Zusammensetzung der Phasen zu beschreiben, z.
Lithiumoxid-Formel, Eigenschaften, Risiken und Verwendungen
Wann lösen sich zwei Stoffe ineinander? Die Löslichkeit ist von der Temperatur abhängig. Die Härte von Lithium beträgt 0,6 auf der Mohs-Skala. Sie bezeichnet die Eigenschaft des Stoffes, sich unter homogener Verteilung (als Atome, Moleküle oder Ionen) im Lösungsmittel zu vermischen, d. Die Löslichkeit von Gasen steigt mit . Sicherheitshinweise GHS-Gefahrstoffkennzeichnung.Für die dann zunehmende Bedeutung von Lithium in Technik und Wissenschaft war dies jedoch von Vorteil.GESTIS-Stoffdatenbank. Gasförmiges Lithiumchlorid bildet . Lithiumfluorid ist in Wasser nur wenig löslich, da die Gitterenergie größer als die Hydratationsenergie ist.Im Gegensatz zu den Carbonaten der übrigen Alkalimetalle ist Lithiumcarbonat in Wasser schwer löslich.
Lithium (Li)
H- und P-Sätze: H: 314: P: 280 ‐ 305+351+338 ‐ 310: Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.Ergebnis: Lösen der Reaktionsprodukte. Die Enthalpie ist – wenn man von Volumenänderungen, also mechanischer Arbeit gegen einen äußeren Druck absieht – gleich der Energie. Enthaltene Ionen: Ba. · Verteilungskoeffizient n-Oktanol/Wasser (log-Wert) Nicht bestimmt. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Sie bezeichnet also die Eigenschaft eines Stoffes, sich unter homogener Verteilung (als Atome, Moleküle oder Ionen) mit dem Lösungsmittel zu vermischen.
Lithiumperoxid
Die Lösung einer starken Säure mit einer Konzentration von 1 M (1 mol/L) hat einen pH-Wert von 0. Dieses hat einen basischen Charakter und deshalb färbt sich das Phenolphthalein rot.Die Löslichkeit des Gases ist vom Druck und von der Temperatur abhängig. Mit zunehmender Temperatur steigt im Allgemeinen die Löslichkeit von festen Stoffen in flüssigen Lösungsmitteln.Bezeichnung des Stoffs Lithiumhydroxid-Monohydrat ≥56,5 % LiOH Artikelnummer 3997 Registrierungsnummer (REACH) 01-2119560576-31-xxxx EG-Nummer 215-183-4 CAS-Nummer 1310-66-3 1. $\ce{Li2O + H2O -> 2 LiOH}$ $\ce{Na2O + H2O -> 2 NaOH}$ $\ce{2 KO2 + 2 H2O -> 2 .
Lithiumhydrid
The substances are listed in alphabetical order. Es hat eine hohe Neigung, Kohlendioxid aus der Luft zu absorbieren. Essigsäure versetzen, dann iumthiocyanat und Amylalkohol hinzugeben. Gefahrenstoffe Kaffeepulver H: – P: – Tee H: – P: – Puderzucker .
Du berechnest ihn, indem du den negativen dekadischen Logarithmus der Säurekonstante bildest. mehrfach im Filter waschen: II.Die Löslichkeit ist von der Temperatur abhängig.Lithiumphosphat ist ein farbloser Feststoff.
Lösungsenthalpie

Der Schmelzpunkt von Lithium beträgt.Löslich in NH 3-Lösung, schwerlöslich in HNO 3 o Cl-+ Ag + → AgCl o AgCl + 2NH 3 → [Ag(NH 3)2]+ + Cl-o [Ag(NH 3)2]Cl + HNO 3 → AgCl + 2 NH 4 + + NO 3-CO 32-o Ansäuern der Ursubstanz mit HCl verd oder HNO 3 verd o CO 2-Entwicklung (Gasblasen, Sprudeln) o Einleiten des entstehenden Gases in Barytwasser(Lösung von Ba(OH)2) oder . Zwar wurde bei 300 °C in geträgertem LiOH molar 1,9 % Ammoniak aufgenommen, während es bei CsOH nur 1,6 % waren.

Die Hochtemperaturvariante besitzt eine Kristallstruktur mit der .Die Lösungsenthalpie oder Lösungswärme ist die Änderung der Enthalpie beim Lösen eines Stoffes in einem Lösungsmittel. In Gegenwart von Säuren zersetzt es sich unter Freisetzung des hochtoxischen Gases Blausäure : Natriumcyanid (20 mg), als weißes Pulver.2 Relevante identifizierte Verwendungen des Stoffs oder Gemischs und Verwendungen, von denen abgeraten wird Relevante identifizierte Verwendungen: . Oxothiometallat-Komplexe. Meist ist das Lösungsmittel eine Flüssigkeit.
Normalerweise schreibt man nur die Ionen auf: LiOH ->Li+ + OH-.Sie gibt dir die Löslichkeit nicht nur als Produkt zweier Ionen-Konzentrationen an, sondern liefert einen realen Wert, wie viel Mol pro Liter eines Salzes im Wasser löslich sind.
Lithiumchlorid
- Lime E Scooter Gps – ILPT Request How to steal a Lime e-bike : r/IllegalLifeProTips
- Lippen Booster Ohne Op | Lippen: So kannst du sie vergrößern
- Linux Mint 20.3 – How to Upgrade to Linux Mint 21 [Step by Step Tutorial]
- Linas Ferienwohnung Sankt Andreasberg
- List Of Tanks In England – Great Britain ground vehicles
- Linux Datei Reparieren | Windows XP reparieren
- Liste Banken Deutschland | Online-Banken-Ranking 2022: Die besten im Vergleich
- Listado De Universidades Europeas
- Liquor Aus Der Nase Austreten , Wie sieht hirnwasser aus?
- Lindt Excellence 100G , EXCELLENCE
- Linguista Sprachaufenthalte : Sprachaufenthalt in Byron Bay
- Lineare Ungleichungen Berechnen
- Liquor Bottle Wikipedia , Bottle service
- Lions Düsseldorf Deutschland – Lions International