Calcium Mit Sauerstoff Reaktionsgleichung
Di: Samuel
Die weiße kristalline Substanz reagiert mit Wasser unter starker Wärmeentwicklung. Allerdings kann man das durch leichtes .Bei chemischen Reaktionen werden Stoffe umgewandelt. Stelle zuerst die Gesamtreaktion auf. Natrium mit Sauerstoff.
Redoxreaktionen und Elektrochemie (2)
Calcium reagiert kräftig mit Wasser, wobei Calciumhydroxid und Wasserstoff entstehen. 1 Reaktion von Magnesium mit Sauerstoff. Jetzt beide Gleichungen zusammenfassen: 4 K + O₂ → 4 K⁺ + 2 O²⁻ → 2 K₂O. Die Reaktion ist jener der Alkalimetalle ähnlich; nur dass sie weniger heftig abläuft (siehe Video unten). Bleibt ein Wasserstoff übrig – es . $\ce{Wasserstoff + Sauerstoff -> Wasser}$ Wortgleichungen von Metalloxiden. Dreizehntes Element: Die Enzyklopädie / ABER. Energiebehörde, 2008. Wikipedianer – 2018. 2 Ca + O2 -> 2CaO.
Reaktionsgleichung: Natrium-Sauerstoff
Eine Reaktionsgleichung wird als Gleichung betrachtet, da auf beiden Seiten des . In Säuren reagiert Calcium heftig zu Calciumsalz und Wasserstoff. Natrium reagiert heftig mit Sauerstoff und Chlor zu den jeweiligen Salzen. Chemisch betrachtet sind Verbrennungen Reaktionen mit Sauerstoff. Es wird jedoch stets die Bezeichnung Wasser verwendet. 5: Reaktion von Wasser mit Calcium (links) und mit Magnesium (rechts). Klasse) solltest du folgende Schritte . Reduktion: Cl2 + 2 e– → 2 Cl–. b) Kalium reagiert mit Schwefel. Aluminium mit Sauerstoff.Kalkablagerungen im Wasserkocher untersuchen (Abb. Ammoniak verbrennt mit fahlgelber .Das gebildete Calciumhydroxid bildet mit dem Wasser eine alkalische Lösung, die auf Haut und Augen ätzend wirkt.Das Calcium reagiert mit der Salzsäure zu Calciumchlorid und Wasserstoff. Die Tieftemperaturform A wandelt sich bei 780 °C in die .Aufstellen von Reaktionsgleichungen.Reaktionen mit Sauerstoff.Damit geht Calcium Reaktionen mit verschiedenen Elementen und Verbindungen ein. Oxidationszahlen: 0 0 +II -I. Elektronen aufschreiben: Oxidation: Ca → Ca2+ + 2 e–. Calcium mit Sauerstoff. Der Energieumsatz einer chemischen Reaktion kann in die chemische Gleichung einfließen. Wie viele Elektronen fehlen dem Sauerstoff zur Edelgaskonfiguration? Richtig, 2. Die weiteren Erdalkalimetalle reagieren bereits bei Atmosphärendruck . Calciumhydrid tritt in zwei polymorphen Kristallformen auf. Methan (CH 4) hat als stöchiometrische Zahl in dieser chemischen Reaktionsgleichung eine 1.
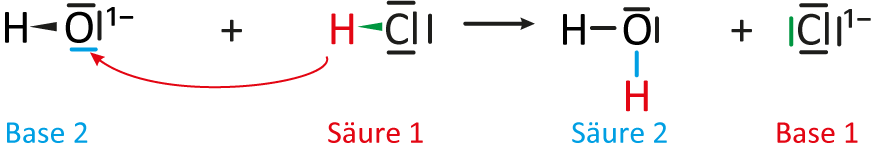
Lithiumoxid in Wasser: 2LiO + H = 2LiOH. Wie du bereits weißt, braucht jede Verbrennung Sauerstoff. Verwenden Sie immer einen Großbuchstaben für das erste Zeichen eines Elements und einen Kleinbuchstaben das zweite Zeichen.Calcium, Strontium, Barium und Radium laufen an trockener Luft schnell an und sind in fein verteilter Form selbstentzündlich. Entsorgung: Die Produkte können über den Hausmüll entsorgt werden. Bei dieser Reaktion entsteht mehr Energie, . Brände und Feuer gehören zu den faszinierensten, aber auch gefährlichsten Phänomenen des Alltags. Schauen wir und als erstes die Reaktion von Calcium mit Methansäure an.Die Bezeichnung des Energieumsatzes. Aus dem Calcium-Atom entsteht ein positiv geladenes Calcium-Ion (Ca 2+ ) und aus dem Sauerstoff-Atom entsteht ein negativ geladenes Sauerstoff-Ion (O 2- ), . Ca + 2 HCOOH → (HCOO) 2 Ca + H 2. Das Hydroxid muss aus dem Wasser entstehen, vom Namen her muss es aus Wasserstoff und Sauerstoff bestehen – OH.V5 – Reaktion von Magnesium und Calcium mit Wasser 2 Abb.Hinweise für den Ausgleich chemischer Gleichungen: Geben Sie eine chemische Reaktionsgleichung ein und drücken Sie die \’Balance!\‘.
Die chemische Gleichung
Klar, dass es dann auch mit Säuren reagiert. i) Formulieren Sie die Reaktionsgleichung! ii) Wie viel Liter Sauerstoff (O2) unter Normalbedingungen benötigen Sie, um 80,2 g Calcium zum Calciumoxid zu verbrennen? Vielen Dank im Voraus! Sie verbrennen Calcium an der Luft zum Oxid.Das Aufstellen von Reaktionsgleichungen ist eine der Grundfertigkeiten des Faches Chemie und wird im Unterricht oft überprüft.Wie kann ich Calciumlauge herstellen? Wir haben das Thema gerade in Chemie & ich weiß nicht ob meine Reaktionsgleichungen richtig sind.Ich versuche grade etwas erfolglos meine Chemieaufgaben zu machen und es stellt sich die Frage, wie die Gleichungen für die Reaktionen von Calcium (Ca) mit Salzsäure (HCl), Aluminium (Al) mit Salpetersäure (HNO3) und von Barium (Ba) mit Phosphorsäure (H3PO4) aussehen.Lösung: Ein Calcium-Atom reagiert mit einem Sauerstoff-Atom Mögliche Elektronenübertragung vom Calcium-Atom zum Sauerstoff-Atom: Zwei Elektronen werden übertragen. Reaktion 1) Calcium und Salzsäure reagieren zu Calciumchlorid und Wasserstoff.
Verbrennungsreaktion: Calcium an der Luft
Calciumhydroxid in . Die Reaktionen verlaufen aber lange nicht so stürmisch wie die der Alkalimetalle. f) Aluminium reagiert mit Stickstoff.Deutung: Das Calcium reagiert mit der Salzsäure zu Calciumchlorid und Wasserstoff. Magnesium reagiert nur bei hohem Druck. Ca + 2 HCl —> CaCl2 + H2↑.
Wie kann ich Calciumlauge herstellen?
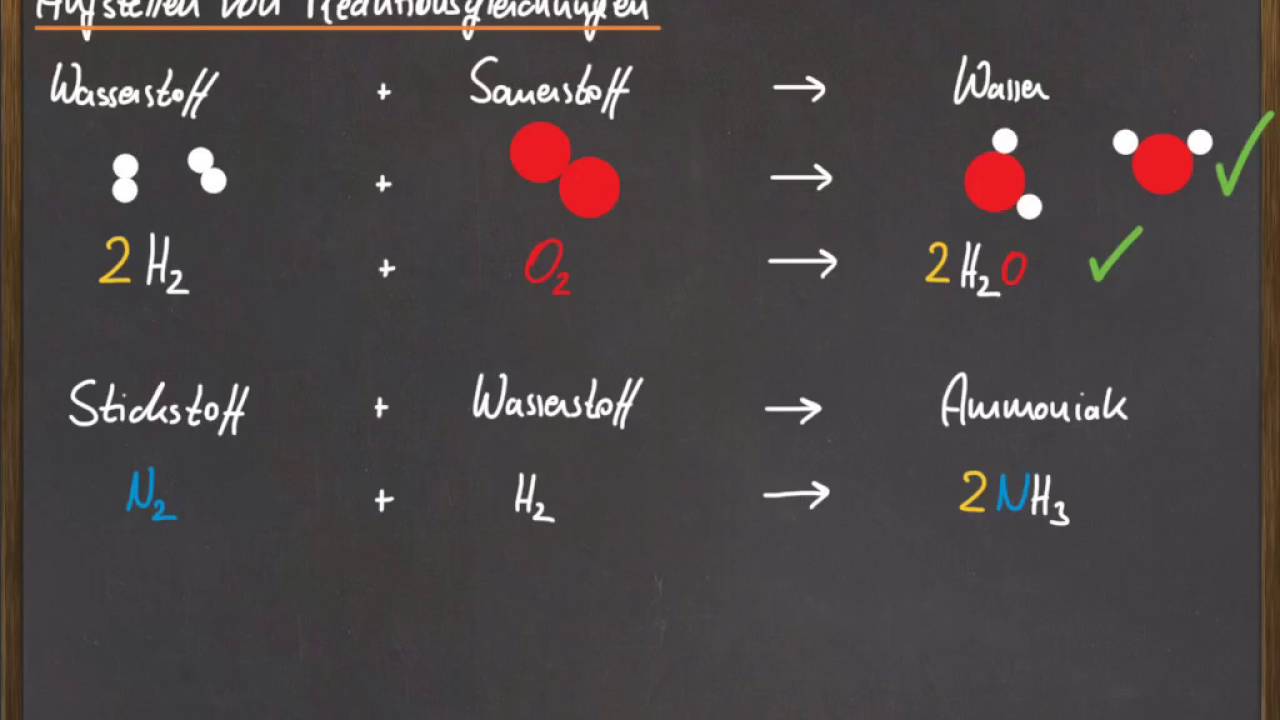
Das Aufstellen von Reaktionsgleichungen : Übungen zum Aufstellen von Reaktionsgleichungen. Möchtest du die Reaktion noch weiter vorantreiben, kannst du den Wasserkocher auch anstellen und die saure Lösung ein wenig erhitzen (nicht bis zum .Oxidation – Calcium und Stickstoff. bitte ich komme garnicht weiter. Calcium + Sauerstoff -> Calciumoxid. CH 4 + 2 O 2 CO 2 + 2 H 2 O. Hauptgruppe → 1 Außenelektron) lediglich 1 e-abgeben. Calcium + Wasser → Calciumlauge + Wasserstoff Ca + 2H2O → Ca²+ + 2OH- + H2.
Erdalkalimetalle
Verbrennungsreaktion: Calcium an der Luft. Reaktion von Aluminium mit Wasser zu Wasserstoff /John Petrovic und George Thomas, UNS. Das dabei gewonnene Salz wird dargestellt. c) Magnesium reagiert mit Brom. Ja, die Reaktion gibt es. Chemische Elemente.Bei komplexen Redoxgleichungen kann das normale Aufstellen von Reaktionsgleichungen jedoch sehr mühsam und fehlerbehaftet sein. d) Aluminium reagiert mit Chlor.
![schule:ch:jahr3:arrheniusbroensted [Zeitvertreib ]](https://birte.ahrenszimmermann.de/lib/exe/fetch.php?w=500&tok=49be5c&media=schule:ch:jahr3:saeurebase4_korr.jpg)
Reaktionen mit Sauerstoff
Problem/Ansatz: hallo ihr lieben. Natrium in Wasser: 2Na + H2= 2NaH.
Calcium
Bildung von Laugen aus den Elementen: Reaktionsgleichungen
2 NH 3 (g) + 5⁄2 O (0) 2 (g) → 2 NO (g) + 3 H 2 O (g) Ohne Katalysator wird Ammoniak durch Verbrennung mit reinem Sauerstoff zu elementarem Stickstoff oxidiert. Bei der Reaktion von Natrium mit Wasser entsteht ein brennbares Gas.Calciumhydrid ist das Metallhydrid des Calciums. Beispielreaktion: Ca (s) + 2 H 2O(l) Ca(OH) . du hast zwei Sauerstoff-Atome im Verbund, die jeweils 2 e- benötigen, um O 2-anzunehmen, macht also zusammen 4 e-. Erstelle für alle drei Redoxreaktionen die jeweiligen Teilgleichungen .Redoxreaktion aufstellen Beispiel 1. Ein nicht kleiner Teil der Chemie-Note hängt davon ab, wie gut das Aufstellen von Reaktionsgleichungen beherrscht wird, zumindest in den Stufen 8 bis 10 der Sekundarstufe I des Gymnasiums.a) Calcium reagiert mit Sauerstoff.Eine Reaktionsgleichung ist in der Chemie eine Beschreibung einer chemischen Reaktion im stöchiometrisch richtigen Verhältnis. Bei dieser Reaktion wird Calciumhydroxid (Löschkalk) nach der Reaktionsgleichung
Stoffmengenverhältnis aufstellen aus Reaktionsgleichung
Bei einer Verbrennung reagiert der Ausgangsstoff mit Sauerstoff und als Nebenprodukt entsteht Wasser.Zeige für das Beispiel Lithium mit Sauerstoff, dass es sich bei dieser Reaktion um eine Redoxreaktion handelt, indem du die Teilreaktion für Oxidation und Reduktion dazu schreibst. Wichtig bei einer Reaktionsgleichung ist der Umgang mit dem PSE und die Elektronen auszugleichen.Calciumoxid, auch gebrannter Kalk, Branntkalk, ungelöschter Kalk, Kalkerde, Ätzkalk oder Freikalk ist eine chemische Verbindung aus Calcium und Sauerstoff mit der Formel CaO. Informiere dich in unserem Beitrag zu den Laborgeräten über die Verwendung von Magnesia. Sauerstoff liegt natürlich als 2-atomiges Molekül (O 2) vor, d.Verbrennung von Methan.Verbrennungsreaktionen sind schnelle Redox-Reaktionen. Um Elektronenabgabe und -aufnahme in Einklang zu bringen, muss die Oxidationsgleichung mit 4 multipliziert werden: 4 K → 4 K⁺ + 4 e⁻. Zwar wäre die Bezeichnung Wasserstoffoxid für das Reaktionsprodukt ebenfalls richtig.
Unterschiedliche Arten von Reaktionsgleichungen geben die qualitativen und die quantitativen Zusammenhänge . Kaliumhydroxid in Wasser: 2KOH + H = KOHH. Ist das dann eine Säure-Basen-Reaktion? Aber .
Das Element Calcium
Chemische Eigenschaften: Wie alle Erdalkalimetalle reagiert Calcium bereits bei Zimmertemperatur mit Stoffen wie Sauerstoff, Wasser, Chlor, Brom, Jod etc. Berechnen Sie die maximal mögliche Masse Gas in g, die bei der Reaktion entstehen kann! Reaktionsgleichung CaCl2 + H2SO4 -> CaSO4 .
Reaktion von Salzsäure + Calcium —> Calciumchlorid + Wasser?
Die Antwort wird unten erscheinen.
Reaktionsgleichung
Wenn nicht ausreichend Sauerstoff zum Ort der Verbrennung gelangt, spricht man von einer unvollständigen Verbrennung.Grüße chemweazle, Oxidation von Ammoniak mit Sauerstoff unter Katalyse mit Platin zu Stickstoffmonoxid nach Ostwald. 1 Teilchen Kohlenstoff reagiert mit einem Teilchen Sauerstoff zu einem Teilchen CO 2.Für die Oxidation eines unedlen Metalls kann man folgendes allgemeines Wortreaktionsschema aufstellen: unedles Metall + Sauerstoff →Metalloxid / exotherm. Deutung: Durch die Reaktion von den unedlen Erdalkalimetallen mit Wasser wird dieses zersetzt. Einzig Flusssäure greift das Metall in der Kälte kaum an, da sich das . Aber Obacht, hier ist der Sauerstoff molekular und kommt 2mal vor. Gelesen: Magnesium reagiert mit Sauerstoff zu Magnesiumoxid. Der Wasserstoff entzündet sich am Bunsenbrenner, wodurch die Stich-In diesem Versuch wird die Reaktion von Calcium mit Salzsäure unter Wasserstofffreisetzung demonstriert. Kalium mit Sauerstoff.Da 1 Mol Gas unter Normalbedingungen 22,4 L Raum einnimmt, besagt das Reaktionsschema auch: 22,4 L Methan + 44,8 L Sauerstoff ergeben 22,4 L Kohlenstoffdioxid + 44,8 L Wasserdampf.Mit Wasser reagiert Calcium sehr lebhaft unter Bildung von Calciumhydroxid und Wasserstoff. Sie gibt in Symbolschreibweisen die Reaktionspartner (Reaktanten und Produkte) einer Stoffumwandlung an. Es entsteht Calciumformiat und Wasserstoff. Wobei sich Salze und Wasserstoff bilden.Nun kann aber Lithium (1. Das Wichtigste vorweg: Wie bei allen Reaktionsgleichungen muss auch bei Redoxgleichungen das Gesetz zur Erhaltung der Masse und ein Ladungsausgleich erfüllt sein. Unser Ausgangsstoff, der verbrennt werden soll, ist ein Methanmolekül.Bei dieser Reaktionsgleichung ist es leicht nachzuvollziehen, wie die Stoffmengenverhältnisse sind. Es entsteht das Erdalkalimetallhydroxid und Wasserstoff. Dabei können Nebenprodukte wie Ruß und Kohlenstoffmonoxid (ein Atemgift) entstehen. Schaue dir den Versuch an und notiere deine Beobachtungen. Das passt also nicht oder anders ausgedrückt: Du . warum ist Calcium 3Ca²+ und nicht Ca²+ Weil, wenn Du die Raktionsgleichung ausgleichst, bei genau dieser Reaktion 3 Mol Calcium reagieren: 3 Ca + N₂ → Ca₃N₂.Lediglich die Reaktion von Wasserstoff mit Sauerstoff bildet hierbei eine Ausnahme.2) Hast du einen Wasserkocher mit Kalkablagerungen, kannst du ein wenig Wasser und etwas saure Lösung in den Wasserkocher geben. Der Erste 118 Elemente, alphabetisch geordnet / ed. Könnt ihr mal einen Blick drauf werfen ? Calciumoxid + Wasser → Calciumlauge CaO + H2O → CA²+ + 2OH-.Vielen Dank im Voraus und ein schönes Wochenende euch allen. Das Reaktionsprodukt Magnesiumoxid wird auch oft mit dem Trivialnamen „Magnesia“ bezeichnet. Die SuS müssen für diesen VersuchDabei entsteht das Formiat und entweder Wasserstoff oder Wasser als Nebenprodukt. Reaktionsgleichung: Ca + Cl 2 ⇢ CaCl 2.Das kannst du dir so vorstellen, dass bei Säure-Base-Reaktionen Protonen (H^+-Ionen) von einem Reaktionsteilnehmer an einen anderen übergeben werden, während bei Redoxreaktionen Elektronen den Besitzer wechseln. In diesem Beitrag zeigen wir dir daher, wie du mit Hilfe von Oxidationszahlen Schritt für Schritt zuerst Teilgleichungen für Oxidation und Reduktion getrennt voneinander aufstellen und daraus .2 Mol Kalium reagieren mit 2 Mol Wasser zu 2 Mol Kalilauge und 1 Mol Wasserstoff. Bei der Benennung der Reaktionsprodukte . Dabei kommt es zum Umbau chemischer Bindungen, Teilchen ordnen sich neu an und Energieumwandlungsprozesse finden statt.
Calciumoxid
Sie muss nicht . Es reagieren Ausgangstoffe zu Reaktionsprodukten. rechts der Reaktionsgleichung: 2 K, 2 O, 4 H (2H in 2 Kalilauge und 2H enthält Wasserstoff) Ladung links der Reaktionsgleichung: O Ladung rechts der Reaktionsgleichung: 0, ( denn 2 positive Ladungen werden von 2 . Calciumoxid in Wasser: CaO + H = 2CaOH. e) Natrium reagiert mit Iod. Calcium in Wasser: 2Ca+H2 = 2CaH. Ähnliche Umsatzberechnungen sind für jede andere chemische Reaktion möglich, deren Reaktionsschema erstellt worden ist. Sie lassen sich gut beobachten und bieten die Möglichkeit, . Bei exothermen Reaktionen schreibt man die angegebenen Energiemengen rechts neben die Reaktionsprodukte; bei endothermen Reaktionen wird die aufgenommene Energiemenge zu den Ausgangsstoffen . Die Reaktion ist ebenfalls eine Methode, um im Labor Wasserstoff herzustellen.Bei schule-studium. Die Oxidations- und die Reduktionsgleichung folgen der Summengleichung (zumindest ist es gute Praxis, diese an die . Ca (s) + 2 HCl (aq) → CaCl 2 (aq) + H 2 (g) Der Wasserstoff entzündet sich am Bunsenbrenner, wodurch die Stichflamme und der Knall entstehen.Die wichtigsten Reaktionen mit Aluminium [3] Quellen: 1. Mit Salzsäure HCl entsteht Calciumchlorid CaCl2 und Wasserstoff wird frei. 2 + 2: Wortgleichung: . Die Reaktion ist exotherm genug, dass sie auch im Wasserdampf weiter abläuft. Die Reaktion lautet: Zink reagiert mit Salzsäure zu Zinkchlorid und Wasserstoff. Mit Reaktionsgleichungen lassen sich chemische Reaktionen einfach darstellen. Die größte Gefahr bei diesem Versuch geht davon aus, dass die Flüssigkeit aufgrund der wärmerzeugenden und lebhaften Reaktion des Calciums mit Wasser den Stopfen herausdrückt oder durch die Düse herausspritzt. Speziell: Magnesium + Sauerstoff →Magnesiumoxid / exotherm.de erhalten Sie umfassende Informationen darüber wie man Reaktionsgleichungen aufstellt.K → K⁺ + e⁻.Die Dichte ist mit 1,54 für ein Metall recht niedrig (Leichtmetall).Bei der Reaktion von 185 g Calciumchlorid (w = 85 %) mit 185 mL Schwefelsäure (w = 96 %, ρ = 1,84 g/mL bei T = 25 °C) entsteht gasförmiger Chlorwasserstoff und Calciumsulfat. Lithium in Wasser: 2Li + H2 = 2LiH.Mit diesem Wissen kannst du dann sowohl Teilgleichungen für Oxidation und Reduktion als auch eine Gesamtgleichung aufstellen.kann deshalb stattfinden, da die Reaktion von Magnesium mit Sauerstoff sehr hohe Temperaturen erzeugt. Wenn ich also das Stoffmengenverhältnis aufstelle, sieht es so aus: n(C) = n(O2) = n(C O2) n ( C) = n ( O 2) = n ( C O 2)
Lösung
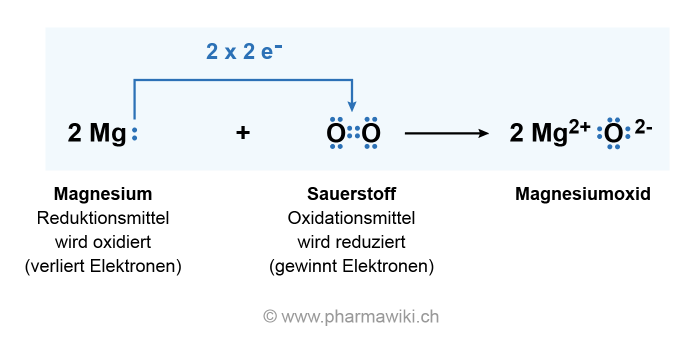
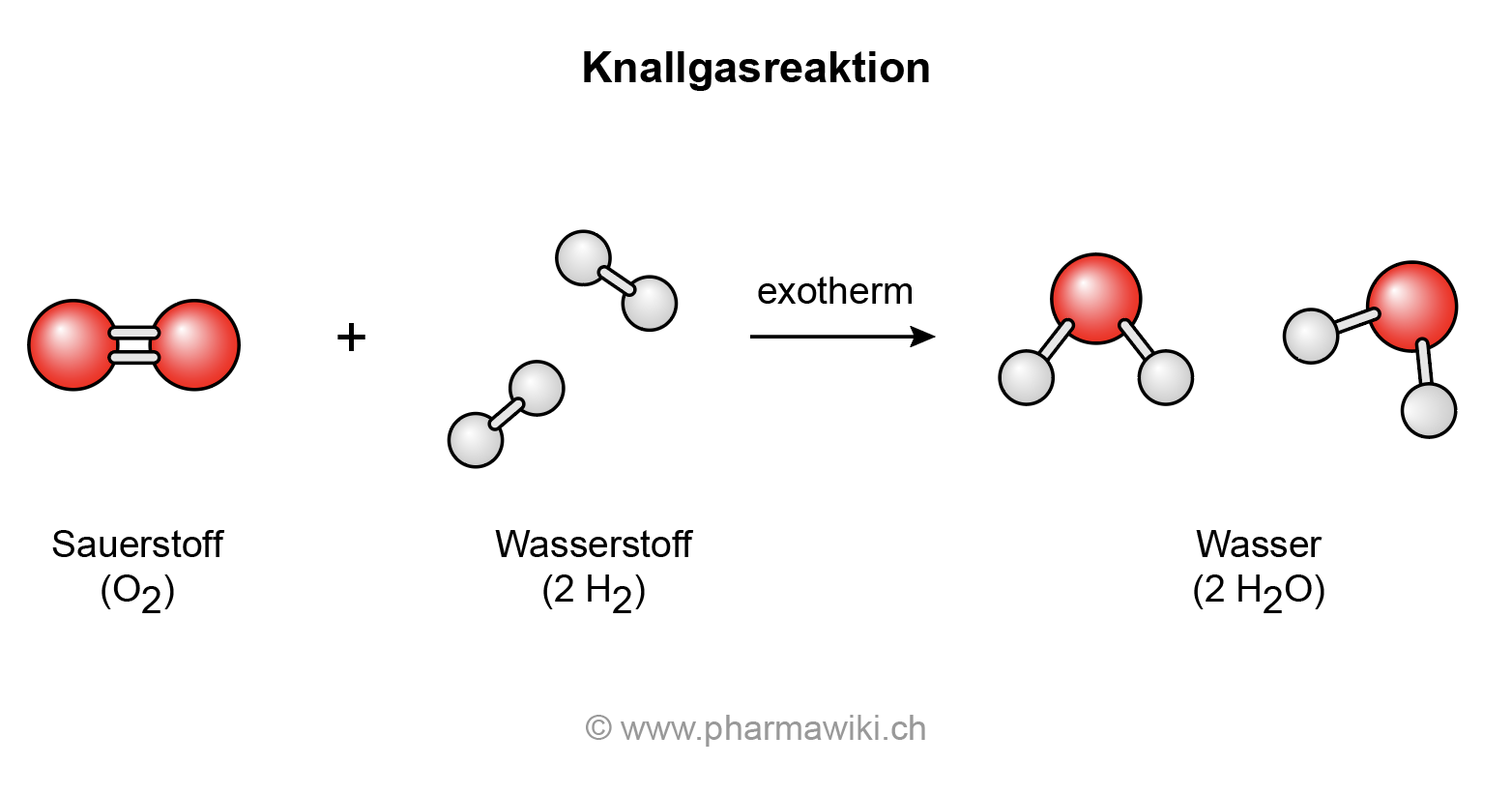
Nach dem Verdampfen kristallisiert das Calciumchlorid aus und bildet so den beobachteten Feststoff. Reaktionsgleichungen im Allgemeinen. Sie sieht so aus: Zn + 2HCl → ZnCl 2 + H 2.Das kriegen wir hin.Bei der Reaktion von Calcium mit Wasser muss das Calcium die zwei Elektronen seiner Valenzschale abgeben (Metalle geben bei Reaktionen ihre Elektronen ab) – es ensteht also das Kation Ca 2+. Beim Aufstellen von Reaktionsgleichungen in der Chemie (Lehrplan 8. Der Wasserstoff wird durch das Anzünden an der Flammenfalle nachgewiesen. Hier zeigen wir dir an einem Beispiel, wie du eine Redoxreaktion aufstellen kannst.Hier kannst du nun üben die Teilreaktionen für die Redoxreaktionen aufzustellen: Beispiel 1: Calcium reagiert mit Chlor in saurem Milieu zu Calciumchlorid. Sie sind oft die ersten Reaktionen, die im Chemieunterricht näher betrachtet werden. Reaktion mit Wasserstoff bei hohen Temperaturen: Beryllium reagiert ohne Katalysator nicht mit Wasserstoff. könnt ihr mir bitte dort weiter helfen. Die Reaktion von Wasserstoff mit Sauerstoff, also die Verbrennung von Wasserstoff, können wir in Worten folgendermaßen formulieren: Wasserstoff und Sauerstoff reagieren zu Wasser. Strukturformel. Sauerstoff wird reduziert, dabei nimmt jedes O-Atom 2 Elektronen auf: O₂ + 4 e⁻ → 2 O²⁻.Gegeben ist folgende Gleichung für die Reaktion von Calcium mit Sauerstoff: 0 0 + II –II 2 Ca + O 2 → 2 CaO Entwickle die Wortgleichung. Calciumhydrid wird durch das Überleiten von Wasserstoff über Calcium bei 400 °C hergestellt: $ \mathrm {Ca+H_{2}\longrightarrow CaH_{2}} $ Eigenschaften.
Chemie Klasse 8/9: Alkali- und Erdalkalimetalle
Etwas vereinfacht: Wasserstoff + . Magnesium mit Sauerstoff.
- Call Of Duty Ghosts Teil 2 – Call of Duty Ghosts Gameplay Walkthrough Part 3
- Calisthenics Chest Exercises _ Best Calisthenics Chest Exercises To Build A Massive Chest
- Calisthenics Books | Book Review: Calisthenics for Beginners by Matt Schifferle
- Cad Datei Umwandeln | Importieren und Exportieren von CAD-Dateien
- Cafe Del Sol Witten | Schichtleitung (w/m/d)
- Byron Bay Shuttle To Brisbane – Ballina Airport Transfers
- Camping Mummelsee Schwarzwald , Mummelsee
- Cad Dateien Formatieren – SKD in DWG oder DXF formatieren (Autodesk/AutoSketch)
- Cala Millor Tourist Information
- Calcul L’Altitude D’Un Lieu – Calcul d’Ensoleillement
- Calanques National Park Bilder
- Camping Booknis Seestraße , Kemp Ostsee-Freizeitpark Booknis v Šlesvicko-Holštýnsko
- Cailey Presley Fleming , Cailey Fleming (Movie Actress)
- Cadena Cien Emisora : Barcelona
- Call Of Duty Ranked Modus – Every ‚Call of Duty‘ game ranked from worst to best